题目内容
11.某固体NaOH因吸收了空气中的少量CO2而含有杂质,现在要将该固体NaOH配制成较纯的溶液,则其主要的实验操作过程应是( )| A. | 溶解 加适量BaCl2溶液 过滤 | |
| B. | 溶解 加适量CaCl2溶液 过滤 | |
| C. | 溶解 加适量Ca(OH)2溶液 过滤 | |
| D. | 溶解 加适量盐酸 加热 |
分析 要将该固体NaOH配制成较纯的溶液,应将混合物中含有的碳酸钠除去,可加入适量的Ca(OH)2溶液,以此解答.
解答 解:题中A、B、D易导致引入新的杂质NaCl,氢氧化钠中混有碳酸钠,可加入适量的Ca(OH)2溶液,然后过滤除去,故C正确.
故选C.
点评 本题考查物质的分离、提纯,侧重于学生的分析能力和实验能力的考查,为高频考点,注意把握物质的性质,除杂时不能引入新的杂质,且不能影响被提纯的物质,难度不大.

练习册系列答案
相关题目
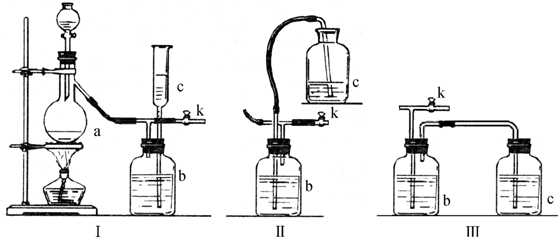
7.8.34g FeSO4•7H2O(分子量:278)样品受热脱水过程的热重曲线(样品质量随温度变化的曲线)如图所示,下列说法正确的是( )

| A. | 温度为78℃时固体物质M的化学式为FeSO4•5H2O | |
| B. | 取适量380℃时所得的样品P,隔绝空气加热至650℃,得到一种固体物质Q,同时有两种无色气体生成,Q的化学式为Fe3O4 | |
| C. | 在隔绝空气条件下,N得到P的化学方程式为FeSO4•H2O $\frac{\underline{\;高温\;}}{\;}$FeSO4+H2O | |
| D. | 温度为l59℃时固体N的化学式为FeSO4•2H2O |
2. 如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )
如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )
 如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )
如图是用高纯度固体二氧化钛生产金属钛的装置示意图,其原理是在较低的电压下,二氧化钛中的氧电离而进入熔融的氯化钙中,最后该电极只剩下纯净的金属钛.已知:熔融状态下,放电强弱为O2->Cl-.下列有关说法正确的是( )| A. | a电极为阴极 | |
| B. | a电极产生的气泡中主要成分是氯气 | |
| C. | 通电时,O2-、Cl-等向阴极移动 | |
| D. | 该制备工艺中需要定期更换石墨棒 |
6.把3mL NO2气体依次通过下列3个分别装有足量的①饱和NaHCO3溶液,②浓硫酸,③Na2O2固体的装置后,用排水法把残留气体收集到集气瓶中,集气瓶内的气体应是( )
| A. | 1 mL NO | B. | 2 mL NO2和0.5 mL O2 | ||
| C. | 2 mL O2 | D. | 0.25 mL O2 |
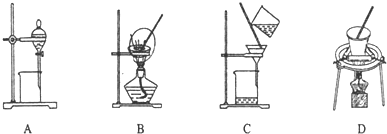
16.某化学兴趣小组设计如下流程,从酸性工业废液(含H+、Al3+、Mg2+、Cr3+、SO${\;}_{4}^{2-}$)中提取铬.

有关数据如表:
回答下列问题:
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).
(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.
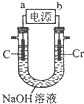
①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)

有关数据如表:
| 化合物 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| 完全沉淀的Ph | 10.5 | 4.3 | 5.3 |
| 开始溶解的pH | -- | 7.8 | 9.2 |
| Ksp近似值 | 10-12 | 10-14 | 10-31 |
(1)步骤①所得滤液可用于制取MgSO4•7H2O,酸性工业废液中加入适量氧化铝的作用是调节溶液的pH.
(2)若酸性废液中c(Mg2+)=0.lmol.L-l,为达到步骤①的实验目的,则废液的pH应保持在(5.3,7.8)范围(保留小数点后l位).
(3)步骤②中生成NaCrO2的离子方程式为Cr(OH)3+OH-=CrO2-+2H2O.
(4)步骤④中反应的离子方程式为7H2O+4CrO42-+6S=4Cr(OH)3↓+3S2O32-+2OH-.
(5)步骤⑤在空气中充分灼烧的目的是使Cr(OH)3完全转化为Cr2O3,可选用的装置是D(填序号).

(6)用如图所示装置制取铬酸钠(Na2CrO4),回答相关问题.

①a是电源的负极,阳极的电极反应式为Cr-6e-+8OH-=CrO42-+4H2O.
②若电解一段时间后阴极收集到标准状况下的气体3.36L,则理论上可制得8.1g铬酸钠(忽略反应2CrO42-(aq)+2H+(aq)?Cr2O72-(aq)+H2O(1)的影响)
3.在FeCl3和CuCl2的混合溶液中加入铁屑,若反应结束后铁有剩余,下列说法正确的是( )
| A. | 溶液中一定存在Fe2+ | B. | 溶液中一定存在Fe3+ | ||
| C. | 溶液中一定存在Cu2+ | D. | 溶液中一定不存在Fe2+ |
20.下列所陈述的事实与解释均正确的是( )
| 选项 | 实验操作及现象 | 实验结论 |
| A | 用pH试纸测定NaClO溶液的酸碱性,试纸显蓝色 | NaClO水解显碱性 |
| B | 收集铜与浓硝酸反应生成的气体,用冰水混合物冷却降温,气体颜色变浅 | 生成的红棕色NO2气体部分转化为无色气体 |
| C | 向某溶液中加入几滴新制的氯水,再加入2滴KSCN溶液,溶液变为红色 | 原溶液中一定含有Fe2+ |
| D | 甲苯能使酸性高锰酸钾溶液褪色 | 发生了萃取 |
| A. | A | B. | B | C. | C | D. | D |