题目内容
一定温度下,在容积为2L的密闭容器中发生反应C0(g)+H20(g) C02(g)+H2(g),部分数据见下表(表中t2>t1):
C02(g)+H2(g),部分数据见下表(表中t2>t1):

下列说法正确的是
A.
反应在t1
min内的平均速率为
B. 平衡时CO的转化率为66.67%
C. 该温度下反应的平衡常数为1
D. 其他条件不变,若起始时n(C0)=0.60 mol, n(H20)= 1.20 mol,则平衡时n(C02)= 0. 20 mol
【答案】
C
【解析】本题考查化学反应速率及化学平衡的有关计算。由反应方程式可知,氢气的平均反应速率等于CO的平衡反应速率,故有v(H2)=v(CO)=(1.2-0.8)/2t1,即,v(H2)=(0.2/t1)mol·L-1·min-1,故A不正确;根据表中数据可知,t2、t1时刻H2O的物质的量相等,说明在t1时刻已达平衡,则平衡时CO的转化率为0.4/1.2=33.3%,故B不正确;平衡常数为K=c(C02)×c(H2)/[c(C0)×c(H20)]=0.4×0.4/(0.8×0.2)=1,C正确;
C0(g)
+ H20(g) C02(g)+ H2(g)
C02(g)+ H2(g)
始量0.60 1.20 0 0
变量 x x x x
平衡0.60-x 1.20- x x x
则有x2/[(0.60-x)×(1.20- x)]=1,解得x=0.4,即n(C02)= 0.40 mol,D不正确

练习册系列答案
相关题目
 一定温度下,在容积为1L的密闭容器中,存在如下关系:xH2O(g)?(H2O)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法不正确的是( )
一定温度下,在容积为1L的密闭容器中,存在如下关系:xH2O(g)?(H2O)x(g),反应物和生成物的物质的量随时间变化关系如图.下列说法不正确的是( )| A、x=3 | ||
| B、该温度下,反应的平衡常数为0.125L3/mol3 | ||
| C、平衡时混合气体的平均摩尔质量是33.3g/mol | ||
D、t1时刻,保持温度不变,再充入1mol H2O(g),重新达到平衡时,
|
在一定温度下,在容积为10L的密闭容器中,用2molCO和10molH2O(气)相互混合并加热到800℃时,有下列平衡:CO+H2O?CO2+H2,且平衡常数K=1,则有CO的转化率为( )
| A、16.7% | B、50% | C、66.7% | D、83.3% |
 一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)?N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答:
一定温度下,在容积为1L的密闭容器内放入2mol N2O4和8mol NO2,发生如下反应:2NO2(红棕色)?N2O4(无色)(△H<0),反应中NO2、N2O4的物质的量随反应时间变化的曲线如图,按下列要求作答: 一定温度下,在容积为V L的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为V L的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示: M
M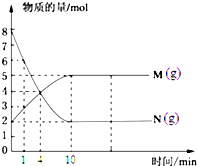 一定温度下,在容积为100L的定容密闭容器中进行某化学反应,反应体系中各组分的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为100L的定容密闭容器中进行某化学反应,反应体系中各组分的物质的量随时间的变化曲线如图所示: