题目内容
14.25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )| A. | 向水中加入少量固体NaHSO4,c(H+)增大,KW不变 | |
| B. | 向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)减小 | |
| C. | 向水中加入少量冰醋酸,平衡正向移动,c(H+) 增大 | |
| D. | 将水加热,KW增大,pH不变 |
分析 水电离生成氢离子、氢氧根离子,所以加入能电离出氢离子或氢氧根离子的物质抑制水电离,加入和氢离子或氢氧根离子反应的物质能促进水电离,温度不变,离子积常数不变,据此分析解答.
解答 解:A、向水中加入硫酸氢钠固体,硫酸氢钠电离出氢离子导致溶液中c(H+)增大,温度不变Kw不变,故A正确;
B、向水中加入氢氧化钠固体,c(OH-)增大,水的电离平衡左移,故B错误;
C、加入少量冰醋酸,溶液中的c(H+) 增大,水的电离被抑制,平衡左移,故C错误;
D、由于水的电离吸热,故将水加热,水的电离平衡右移,Kw增大,溶液中的c(H+)增大,故pH减小,故D错误.
故选A.
点评 本题考查离子积常数、水的电离,明确氢离子或氢氧根离子抑制水电离、弱离子促进水电离即可解答,注意离子积常数与溶液酸碱性无关,置于温度有关,为易错点.

练习册系列答案
 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案
相关题目
4.下列应用不涉及氧化还原反应的是( )
| A. | Na2O2用作呼吸面具的供氧剂 | B. | 工业上电解熔融状态Al2O3制备Al | ||
| C. | 工业上利用合成氨实现人工固氮 | D. | 实验室用NH4Cl 和Ca(OH)2制备NH3 |
5.人工光合系统装置(如图)可实现以CO2和H2O合成CH4.下列有关说法不正确的是( )

| A. | 该装置为原电池,且铜为正极 | |
| B. | 电池工作时,H+向Cu电极移动 | |
| C. | GaN电极表面的电极反应式为:2H2O-4e-═O2+4H+ | |
| D. | 反应CO2+2H2O═CH4+2O2中每消耗1mol CO2转移4mol e- |
2.某工厂排放的工业废水中可能含有K+、Al3+、NH4+、Mg2+、SO42-、Cl-、NO3-、HCO3-等离子.经检测废水呈明显的碱性,则可确定该厂废水中肯定不大量含有的离子组合是( )
| A. | Al3+、NH4+、Mg2+、HCO3- | B. | K+、NH4+、NO3-、SO42- | ||
| C. | Al3+、K+、NO3-、HCO3- | D. | K+、Mg2+、SO42-、Cl- |
19.向甲溶液中缓慢滴加乙溶液,反应生成沉淀的质量与乙溶液的量之间的关系如图所示,其中符合图象的是( )
| 甲 | 乙 | 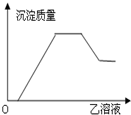 | |
| A | AlCl3、Mg(NO3)2、HNO3 | NaOH | |
| B | Na2CO3、NH4HCO3、Na2SO4 | Ba(OH)2 | |
| C | NH4NO3、Al(NO3)3、Fe(NO3)3、HCl | NaOH | |
| D | NaAlO2、氨水、NaOH | H2SO4 |
| A. | A | B. | B | C. | C | D. | D |
6.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 大量排放氮氧化物可以形成酸雨、产生光化学烟雾,威胁人类生活环境 | |
| B. | 食用地沟油对人体危害大,但地沟油可用来制肥皂 | |
| C. | 明矾水解可生成Al(OH)3胶体,常用于水的杀菌消毒 | |
| D. | 人们可利用元素周期律在过渡元素中寻找性能优良的催化剂 |
3.下列说法正确的是( )
| A. | C60的摩尔质量是720 | |
| B. | 金刚石、石墨和C60互为同位素 | |
| C. | 因石墨具有导电性,可用石墨炸弹破坏输电线、电厂设备 | |
| D. | 在点燃的条件下,碳可以还原氧化镁生成镁和二氧化碳 |
4.三氯化磷(PCl3)是一种重要的掺杂剂.实验室要用黄磷(即白磷)与干燥的Cl2模拟工业生产制取PCl3,装置如图所示:(部分夹持装置略去)
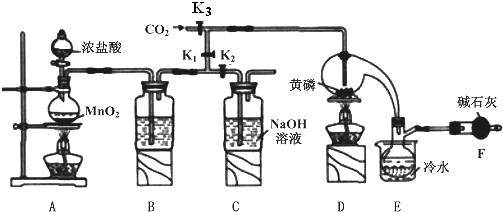
已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
请回答下列问题:
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.

已知:①黄磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5;
②PCl3遇水会强烈水解生成 H3PO3和气体;
③PCl3遇O2会生成POCl3,POCl3溶于PCl3;
④PCl3、POCl3的熔沸点见下表:
| 物质 | 熔点/℃ | 沸点/℃ |
| PCl3 | -112 | 75.5 |
| POCl3 | 2 | 105.3 |
(1)B中所装试剂是浓硫酸;
E中冷水的作用是冷凝PCl3防止其挥发.
(2)F中碱石灰的作用是吸收多余的氯气,防止空气中的水蒸汽进入烧瓶中和PCl3 反应.
(3)实验时,检查装置气密性后,先打开K3通入干燥的CO2,再迅速加入黄磷.通干燥CO2的作用是排尽装置中的空气,防止白磷自燃.
(4)粗产品中常含有POC13、PCl5等.加入黄磷加热除去PCl5后,通过蒸馏(填实验操作名称),即可得到较纯净的PCl3.
(5)实验结束时,可以利用C中的试剂吸收多余的氯气,C中反应的离子方程式为Cl2+2OH-=Cl-+ClO-+2H2O.
(6)通过下面方法可测定产品中PCl3的质量分数:
①迅速称取1.00g产品,加水反应后配成250mL溶液;
②取以上溶液25.00mL,向其中加入10.00mL 0.1000mol/L碘水,充分反应;
③向②所得溶液中加入几滴淀粉溶液,用0.1000mol/L的Na2S2O3,溶液滴定;
④重复②、③操作,平均消耗Na2S2O3溶液8.40mL.
已知:H3PO3+I2=H3PO4+2HI,I2+2Na2S2O3═2NaI+Na2S4O6,根据上述数据,假设测定过程中没有其他反应,该产品中PCl3的质量分数为79.75%.
