题目内容
5.下列有关叙述不正确的是( )| A. | 不需要通过化学反应就能从海水中获得食盐和淡水 | |
| B. | 潜水艇在紧急情况下可用过氧化钠供氧 | |
| C. | 氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 | |
| D. | 工业上常用硅制造光导纤维;用铝粉还原一些金属氧化物来制金属 |
分析 A、根据氯化钠溶解度随温度变化不大,利用蒸发溶剂方法得到氯化钠,淡水是蒸馏方法得到;
B、过氧化钠可以与二氧化碳生成氧气;
C、氯气和碱反应得到次氯酸盐,进一步反应生成次氯酸据有杀菌消毒作用;
D、光导纤维是石英的晶体,成分是二氧化硅;
解答 解:A、海水中获得食盐和淡水的方法是通过蒸发溶剂、蒸馏等物理过程实现,故A正确;
B、过氧化钠与二氧化碳反应会生成氧气,提供呼吸需要的氧气,故B正确;
C、氯气和烧碱反应得到次氯酸钠溶液,水解生成次氯酸具有消毒作用,氯气和石灰乳反应生成的次氯酸钙是漂白粉的有效成分,会生成次氯酸具有杀菌消毒作用,故C正确;
D、光导纤维是用二氧化硅制成的,故D错误;
故选D.
点评 本题考查了海水晒盐、得到淡水的原理,氯气、过氧化钠、二氧化硅的性质应用,题目难度中等.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
15. 冬青油结构如图,它在一定条件下能发生的反应有:( )
冬青油结构如图,它在一定条件下能发生的反应有:( )
①加成反应
②水解反应
③消去反应
④取代反应
⑤与NaHCO3反应放出CO2
⑥加聚反应.
 冬青油结构如图,它在一定条件下能发生的反应有:( )
冬青油结构如图,它在一定条件下能发生的反应有:( )①加成反应
②水解反应
③消去反应
④取代反应
⑤与NaHCO3反应放出CO2
⑥加聚反应.
| A. | ①②⑥ | B. | ①②③ | C. | ④⑤⑥ | D. | ①②④ |
16.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 分别加热Na2CO3和NaHCO3固体 | 试管内壁都有水珠 | 两种物质均 受热分解 |
| B | 向FeSO4溶液中先滴入KSCN溶液再滴加H2O2溶液 | 加入H2O2后溶液变成血红色 | Fe2+既有氧化性又有还原性 |
| C | 向漂白粉中滴入稀硫酸,将生成的气体通入品红溶液 | 品红溶液褪色 | 气体中含有Cl2 |
| D | 向含I-的无色溶液中滴加少量新制氯水,再滴加淀粉溶液 | 加入淀粉后溶液变成蓝色 | 还原性:Cl->I- |
| A. | A | B. | B | C. | C | D. | D |
10.常温时向0.01mol/L 的盐酸溶液中加入等体积的下列溶液,滴入酚酞试液显红色,该溶液是( )
| A. | pH=12的Ba(OH)2溶液 | B. | pH=12的氨水 | ||
| C. | 0.01mol/L AgNO3溶液 | D. | 0.005mol/L NaOH溶液 |
17. 碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
(1)某学生的实验流程如下:

①称量用的仪器是托盘天平,最小量度单位0.1g.
②如图为灼烧装置.下列对应仪器的名称中,若正确的在后面横线上写上“正确”,若错误请将正确名称写在后面横线上.
a.坩锅正确 b.三脚架泥三角
③流程中“操作”是指冷却,这一操作必须放在干燥器(填仪器名称)中进行.
④该学生停止实验的依据为连续两次称量的质量差不超过0.1g.
⑤实验结果记录如下:容器质量为33.6g
根据上表数据推算出n值,n=10.
(2)另有学生测定结果n值偏小,其可能的原因为b、c.
a.温度过高致少量碳酸钠分解了 b.碳酸钠晶体样品已有少量风化
c.碳酸钠晶体样品没有完全失去结晶水 d.加热过程中有少量晶体溅出.
 碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.
碳酸钠在不同温度下可以失去部分或全部的结晶水,现有一种碳酸钠晶体(Na2CO3•nH2O)样品,可采用在不同温度下加热样品(温度逐渐升高)来测定其组成.(1)某学生的实验流程如下:

①称量用的仪器是托盘天平,最小量度单位0.1g.
②如图为灼烧装置.下列对应仪器的名称中,若正确的在后面横线上写上“正确”,若错误请将正确名称写在后面横线上.
a.坩锅正确 b.三脚架泥三角
③流程中“操作”是指冷却,这一操作必须放在干燥器(填仪器名称)中进行.
④该学生停止实验的依据为连续两次称量的质量差不超过0.1g.
⑤实验结果记录如下:容器质量为33.6g
| 称量次序 | 加热温度(℃) | 容器+试样质量(g) |
| Ⅰ | 常温 | 62.2 |
| Ⅱ | T1 | 56.8 |
| Ⅲ | T2 | 49.6 |
| Ⅳ | T3 | 44.2 |
| Ⅴ | T4 | 44.2 |
(2)另有学生测定结果n值偏小,其可能的原因为b、c.
a.温度过高致少量碳酸钠分解了 b.碳酸钠晶体样品已有少量风化
c.碳酸钠晶体样品没有完全失去结晶水 d.加热过程中有少量晶体溅出.
14.在密闭容器里,A与B反应生成C,其反应速率分别用vA、vB、vC表示,已知vB=3vA,3vC=2vB,则此反应可表示为( )
| A. | 2 A+3 B→2 C | B. | A+3 B→2 C | C. | 3 A+B→2 C | D. | A+B→C |
15.如图所示,甲池的总反应式O2+N2H4═2H2O+N2.有关该装置工作时,说法正确的是( )
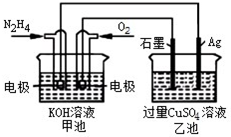

| A. | 甲池中,负极反应为N2H4-4e-═4H++N2 | |
| B. | 甲池溶液pH 保持不变,乙池溶液pH 减小 | |
| C. | 甲池中消耗2.24LO2,此时乙池中理论上多产生12.8g 固体 | |
| D. | 反应一段时间后,向乙池中加一定量CuO 固体,能使CuSO4溶液恢复到原浓度 |