题目内容
化学与生活、生产联系密切,下列说法不正确的是( )
| A、生石灰、铁粉常用于食品干燥剂 |
| B、“地沟油”经过加工处理后可用来制肥皂 |
| C、抗酸药如小苏打可治疗因胃酸过多引起的消化不良 |
| D、以粮食为原料酿酒过程的变化包括粮食一淀粉一葡萄糖一乙醇 |
考点:常见的食品添加剂的组成、性质和作用,油脂的性质、组成与结构,淀粉的性质和用途,药物的主要成分和疗效
专题:化学应用
分析:A.铁粉不吸收水,不能作干燥剂;
B.“地沟油”的主要成分是高级脂肪酸甘油酯,根据其性质分析;
C.小苏打能与胃酸中的HCl反应;
D.根据粮食酿酒的过程分析.
B.“地沟油”的主要成分是高级脂肪酸甘油酯,根据其性质分析;
C.小苏打能与胃酸中的HCl反应;
D.根据粮食酿酒的过程分析.
解答:
解:A.铁粉不吸收水,不能作干燥剂,生石灰能吸水,可用作干燥剂,故A错误;
B.“地沟油”的主要成分是高级脂肪酸甘油酯,高级脂肪酸甘油酯在碱性条件下发生皂化反应,生成肥皂,故B正确;
C.小苏打能与胃酸中的HCl反应,所以抗酸药如小苏打可治疗因胃酸过多引起的消化不良,故C正确;
D.粮食中淀粉含量较高,淀粉在一定条件下水解生成葡萄糖,葡萄糖在酒化酶作用下生成酒精,故D正确.
故选A.
B.“地沟油”的主要成分是高级脂肪酸甘油酯,高级脂肪酸甘油酯在碱性条件下发生皂化反应,生成肥皂,故B正确;
C.小苏打能与胃酸中的HCl反应,所以抗酸药如小苏打可治疗因胃酸过多引起的消化不良,故C正确;
D.粮食中淀粉含量较高,淀粉在一定条件下水解生成葡萄糖,葡萄糖在酒化酶作用下生成酒精,故D正确.
故选A.
点评:本题考查了化学知识在生产生活中的应用,题目涉及的知识点较多,侧重于基础知识的考查,难度不大.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
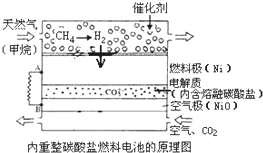 以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池如图,下列说法不正确的是( )
以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池如图,下列说法不正确的是( )| A、外电路电子流动方向:由A流向B |
| B、空气极发生反应的离子方程式是O2+4e-=2O2- |
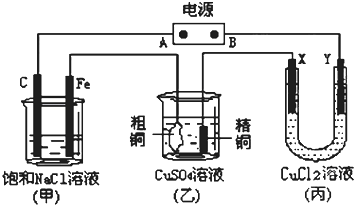
| C、以此燃料电池为电源电解精炼铜,当电路有0.6mol e?转移,有19.2g精铜析出 |
| D、负极反应为H2-2e-+CO32-=CO2+H2O |
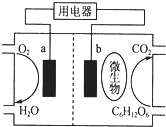 以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )
以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )| A、该电池能够在高温下工作 |
| B、b电极发生还原反应 |
| C、O2在a电极被氧化 |
| D、电流从a电极经用电器流向b电极 |
NA表示阿伏加德罗常数的值,下列叙述中不正确的是( )
| A、Fe与标准状况下2.24L Cl2恰好完全反应,转移电子数目为0.2NA |
| B、0.5mol Na2O2和0.5mol Na2O组成的混合物中,含阴离子数目为1.5NA |
| C、17g NH3分子中含有的共用电子对数为3NA |
| D、1.7g OH-所含电子总数为NA |
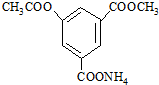 某有机物的结构简式如图所示,该物质1mol与足量NaOH溶液充分反应,消耗NaOH物质的量为( )
某有机物的结构简式如图所示,该物质1mol与足量NaOH溶液充分反应,消耗NaOH物质的量为( )| A、5mol | B、4mol |
| C、3mol | D、2mol |
下列离子方程式正确的是( )
| A、硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ |
| B、金属钾与水反应:K+2H2O═K++2OH-+H2↑ |
| C、碳酸氢钙溶液中加入少量氢氧化钠溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═2HClO+CaSO3↓ |
 有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:
有一未知的无色溶液,只可能含有以下离子中的若干种(忽略由水电离产生的H+、OH-):H+、NH4+、K+、Mg2+、Cu2+、Al3+、NO3-、CO32-、SO42-,现取三份100mL溶液进行如下实验:①第一份加足量AgNO3溶液后,有白色沉淀产生.
②第二份加足量BaCl2溶液后,有白色沉淀产生,经洗涤、干燥后,沉淀质量为6.99g.
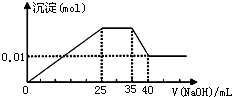
③第三份逐滴滴加NaOH溶液,测得沉淀与NaOH溶液的体积关系如图.根据上述实验,以下推测不正确的是( )
| A、原溶液一定不存在H+、Cu2+、CO32- |
| B、不能确定原溶液是否含有K+、NO3- |
| C、实验所加的NaOH的浓度为2mol?L-1 |
| D、原溶液确定含Mg2+、Al3+、NH4+,且n(Mg2+):n(Al3+):n(NH4+)=1:1:2 |
下列物质分类正确的是( )
| A、SO2、CO均为酸性氧化物 |
| B、硅酸、氯化铁溶液均为胶体 |
| C、烧碱、盐酸均为电解质 |
| D、水玻璃、氨水均为混合物 |