题目内容
在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小28.5%.下列说法正确的是( )
| A、前2min SO2的平均反应速率0.01425mol(L?s) | B、平衡时,SO2的浓度为0.01425mol/L | C、平衡时,SO2的转化率为95% | D、平衡时,SO2的转化率为71.5% |
分析:依据化学平衡三段式列式计算,设二氧化硫转化物质的量为x,则
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
变化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
气体物质的量之比和气体压强之比分析判断计算;
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
变化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
气体物质的量之比和气体压强之比分析判断计算;
解答:解:在500℃时,把0.3mol SO2和0.2mol O2充入一个体积为10L并盛有V2O5(催化剂)的真空密闭容器中,保持温度不变,经2min后,容器内的压强不再变化,此时容器内压强减小28.5%,设二氧化硫转化物质的量为x,则
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
变化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
容器内的压强不再变化,此时容器内压强减小28.5%,即气体物质的量减少28.5%,得到(0.3+0.2)×(1-28.5%)=0.3-x+0.2-0.5x+x
x=0.285mol
A、前2min SO2的平均反应速率=
=0.01425mol(L?min),故A错误;
B、平衡时,SO2的浓度为=
=0.0285mol/L,故B错误;
C、平衡时,SO2的转化率=
×100%=95%,故C正确;
D、平衡时,SO2的转化率=
×100%=95%,故D错误;
故选C.
2SO2+O2 =2SO3
起始量(mol) 0.3 0.2 0
变化量(mol) x 0.5x x
平衡量(mol)0.3-x 0.2-0.5x x
容器内的压强不再变化,此时容器内压强减小28.5%,即气体物质的量减少28.5%,得到(0.3+0.2)×(1-28.5%)=0.3-x+0.2-0.5x+x
x=0.285mol
A、前2min SO2的平均反应速率=
| ||
| 2min |
B、平衡时,SO2的浓度为=
| 0.285mol |
| 10L |
C、平衡时,SO2的转化率=
| 0.285mol |
| 0.3mol |
D、平衡时,SO2的转化率=
| 0.285mol |
| 0.3mol |
故选C.
点评:本题考查了化学平衡三段式计算应用,反应速率、转化率、平衡浓度计算分析应用是解题关键,题目难度中等.

练习册系列答案
相关题目
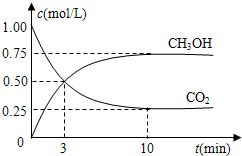
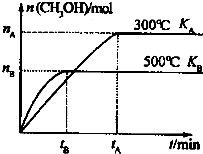 CO和H2与我们的生产和生活等方面密切相关.
CO和H2与我们的生产和生活等方面密切相关.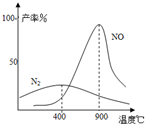 (2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下:
(2009?中山模拟)工业合成氨与制备硝酸一般可连续生产,流程如下: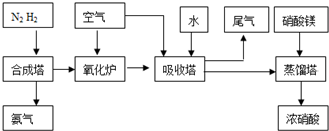

 研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题:
研究CO、NO、NO2等气体的性质,以便消除污染或变废为宝,可以保护环境、节约资源.试运用所学知识,解决下列问题: