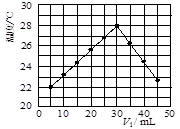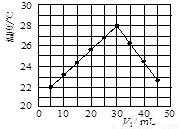题目内容
某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:

(1)研究小组做该实验时环境温度 (填“高于”、 “低于”或“等于”)22 ℃.
(2)由题干及图形可知,V1︰V2= 时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为 mol/L。
(3)实验时将酸碱在简易量热计中混合,并用 搅拌,使溶液混合均匀。经有关计算
知此反应共放出Q kJ的热量,请写出此反应的热化学方程式: 。
【答案】
(1)低于;(2)3︰2;1.5mol·L-1
(3)环形玻璃搅拌棒;H+(aq) + OH-(aq)=H2O (aq)△H = -100 Q / 3 kJ·mol-1或HCl(aq) + NaOH(aq)=NaCl(aq)+H2O (l)△H = -100 Q /3 kJ·mol-1
【解析】酸碱中和放热,低于22℃。V1︰V2=3︰2时,酸碱恰好完全中和,中和时消耗酸30ml,碱20ml反应所用NaOH溶液的浓度应为1.5mol/L。
环形玻璃搅拌棒;H+(aq) + OH-(aq)=H2O (aq)△H = -100 Q / 3 kJ·mol-1

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
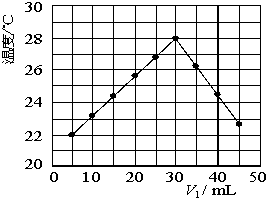 某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL).回答下列问题:
某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL).回答下列问题: 某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题:
某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).回答下列问题: