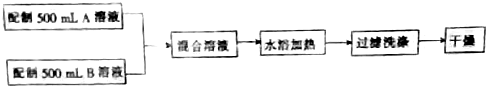
题目内容
2.实验中的下列操作正确的是( )| A. | 用试管取出试剂瓶中的Na2CO3溶液,发现取量过多为了不浪费,又把过量的试剂倒入试剂瓶中 | |
| B. | Ba(NO3)2溶于水,可将含有Ba(NO3)2的废液倒入水槽中,再用水冲入下水道 | |
| C. | 用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | 酒精灯不慎碰翻着火时可用湿抹布盖灭 |
分析 A.取出Na2CO3溶液,发现取量过多,不能放回原瓶;
B.钡离子有毒;
C.蒸发时利用余热加热;
D.隔绝氧气或空气,可以灭火.
解答 解:A.取出Na2CO3溶液,发现取量过多,不能放回原瓶,会污染原试剂,故A错误;
B.钡离子有毒,则Ba(NO3)2 的废液不能用水冲入下水道,防止污染地下水,故B错误;
C.蒸发时利用余热加热,则将蒸发皿中NaCl 溶液蒸发到大量晶体出现时停止加热,故C错误;
D.实验室酒精灯中酒精灯不慎碰翻着火,迅速用湿布盖灭,湿布在降温同时也隔绝氧气而灭火,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及实验基本操作和实验安全等,注重实验基本技能的考查,注意选项B中钡离子有毒,题目难度不大.

练习册系列答案
 小学课时特训系列答案
小学课时特训系列答案
相关题目
12.下列各组物质中,所含分子数不相同的是( )
| A. | 1molO2和1molH2 | B. | 5.6LN2(标准状况下)和11gCO2 | ||
| C. | 224mLH2(标准状况下)和0.1molN2 | D. | 9gH2O和0.5molBr2 |
10.下列溶液中的c(Cl-)与50mL 1mol/L氯化铝溶液中的c(Cl-)相等的是( )
| A. | 150mL 1mol/L氯化钠溶液 | B. | 75mL 2mol/L氯化镁溶液 | ||
| C. | 150mL 1.5mol/L氯化钾溶液 | D. | 75mL 1mol/L氯化铁溶液 |
7.已知反应:
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
①101kPa时,2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1
②稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列结论正确的是( )
| A. | 碳的燃烧热大于110.5 kJ•mol-1 | |
| B. | 2C(g)+O2(g)═2CO(g)△H>-221 kJ•mol-1 | |
| C. | 98%的浓硫酸与稀氢氧化钠溶液反应生成1mol水的中和热为-57.3kJ•mol-1 | |
| D. | 稀醋酸与稀氢氧化钠溶液反应生成1mol水时放出57.3kJ的热量 |
14.鉴别甲苯、己烯、苯酚溶液、丙烯酸溶液、乙醇,可选用的试剂是( )
| A. | KMnO4溶液、FeCl3溶液 | B. | 溴水、KMnO4溶液 | ||
| C. | NaOH溶液、FeCl3溶液 | D. | 溴水、Na2CO3溶液 |
1.下列说法错误的是( )
| A. | 浓硫酸具有强氧化性,但SO2气体可以用浓硫酸干燥 | |
| B. | 常温下实验室可以用稀硝酸与铁反应制取NO气体 | |
| C. | 王水溶解金的过程为氧化还原反应,还原产物为NO2 | |
| D. | SiO2不仅能与氢氧化钠溶液反应,也能与氢氟酸反应 |
 实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示).
实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示).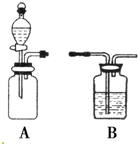 如图是中学化学中常见的实验装置.
如图是中学化学中常见的实验装置.