题目内容
已知:N2(g)+3H2(g)![]() 2NH3(g)+Q,2SO2(g)+O2(g)
2NH3(g)+Q,2SO2(g)+O2(g)![]() 2SO3(g)+Q回答下列问题:
2SO3(g)+Q回答下列问题:
(1)从影响速率和平衡的因素分析,要有利于NH3和SO3的生成,理论上应采取的措施是________.实际生产中采取的措施分别是________.
(2)在实际生产合成氨过程中,要分离出氨气,目的是________;而合成SO3过程中,不需要分离出SO3,原因是________.
答案:
解析:
解析:
|
答案:(1)高温、高压、催化剂;合成氨:适宜的温度、高压、催化剂,合成SO3:高温、常压、催化剂 (2)减小生成物浓度,使平衡向生成NH3方向移动;该反应向SO3生成的方向进行程度大,达到平衡后SO2余量较少,故不需要分离SO3 解析:(1)实际措施中的区别是合成氨采用高压而合成SO3采取常压,这是因为常压时SO2的转化率已很高(SO3占91%),再采取高压受动力、设备等限制,使成本高不经济. (2)合成氨中NH3易液化便于分离;合成SO3中,SO2转化率高,生成SO3相当多,不需要分离SO3,也不方便分离. |

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目


 2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。
2NH3(g)。在一定温度下,将一定量的N2和H2通入固定体积为1L的密闭容器中达到平衡后,改变下列条件,能使平衡向正反应方向移动的是 。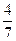 。计算该条件下达到平衡时N2转化率为 ;
。计算该条件下达到平衡时N2转化率为 ;