��Ŀ����
������Ԫ��A��B��C��D��E��F��G�������������������࣬Aԭ����Ԫ���е����������ٵģ�B�������������Ǵ����������Ķ�����C����������������Ӳ�����������G��Cͬ������Ԫ�غ����������֮����D��E��Ԫ�غ����������֮����ȣ�F������������Ǵ����������Ķ���֮һ��
(1)��д��Ԫ��F�����ڱ��е�λ��________��
(2)����Ԫ��ABC��ɵ�18�������ʣ��Ǽپ��г������ж�����֮һ�������ʽΪ________��
(3)����֪��������ӦG(s)��C2(g) GC2(g)����H1����296 KJ��mol��1��2GC3(g)
GC2(g)����H1����296 KJ��mol��1��2GC3(g)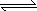 2GC2(g)��C2(g)����H2����198 KJ��mol��1
2GC2(g)��C2(g)����H2����198 KJ��mol��1
��2G(s)��3C2(g)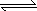 2GC3(g)����H3��________��
2GC3(g)����H3��________��
(4)�����ڿ��淴Ӧ��2GC2(g)��C2(g)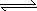 2GC3(g)����H��a KJ��mol��1ͼ���������߷ֱ��ʾ�¶�ΪT1��T2ʱ��ϵ��GC3�İٷֺ�����ʱ��Ĺ�ϵ��
2GC3(g)����H��a KJ��mol��1ͼ���������߷ֱ��ʾ�¶�ΪT1��T2ʱ��ϵ��GC3�İٷֺ�����ʱ��Ĺ�ϵ��
GC3��
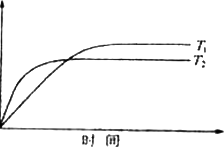
T1ʱƽ�ⳣ��K1��T2ʱƽ�ⳣ��K2����K1________K2(����������)��
T2ʱ��2 L�ܱ������г���4 moL��GC2��3 moL��C2����һ�������´ﵽƽ��ʱGC2��ת����Ϊ90��������ʱ��ƽ�ⳣ����ֵ��________��
(5)��D2FC3��Һ��E2(GC4)3��Һ��ϲ�������������DCA��Һ���������ʣ�д������Һ��������������ӷ�Ӧ����ʽ________��
(6)��Ba(AGC3)2��Һ�еμ�����A2C2����23.3�˰�ɫ����ʱ����Ӧ�е���ת���������ʵ���Ϊ________��
������
|
����(1)��3���ڵڢ�A�� ����(2) ����(3)��H3����790 KJ��mol��1 ����(4)����135 ����(5)3SiO32����2Al3+��6H2O ����(6)0.4 mol |


 2Al(OH)3����3H2SiO3��
2Al(OH)3����3H2SiO3��