题目内容
下列关于金属钠性质和保存的叙述中,正确的是( )
| A、钠是密度小、硬度大、熔点高的银白色金属 |
| B、钠在纯净的氧气中充分燃烧,生成白色固体Na2O |
| C、将金属钠放入CuSO4溶液中,可观察到大量红色的铜析出 |
| D、实验室中,少量的金属钠保存在盛有煤油的广口试剂瓶中 |
考点:钠的化学性质
专题:金属概论与碱元素
分析:A.Na质软,熔点低;
B.Na燃烧生成过氧化钠;
C.Na与水反应生成NaOH,再与CuSO4反应生成氢氧化铜;
D.钠与煤油不反应,且密度比煤油的大.
B.Na燃烧生成过氧化钠;
C.Na与水反应生成NaOH,再与CuSO4反应生成氢氧化铜;
D.钠与煤油不反应,且密度比煤油的大.
解答:
解:A.钠是密度小、质软,熔点低的银白色金属,故A错误;
B.钠在纯净的氧气中充分燃烧,生成淡黄色固体Na2O2,故B错误;
C.Na与水反应生成NaOH,再与CuSO4反应生成蓝色氢氧化铜沉淀,则不会观察到大量红色的铜析出,故C错误;
D.钠与煤油不反应,且密度比煤油的大,则实验室中,少量的金属钠保存在盛有煤油的广口试剂瓶中,隔绝空气防止Na被氧化,故D正确;
故选D.
B.钠在纯净的氧气中充分燃烧,生成淡黄色固体Na2O2,故B错误;
C.Na与水反应生成NaOH,再与CuSO4反应生成蓝色氢氧化铜沉淀,则不会观察到大量红色的铜析出,故C错误;
D.钠与煤油不反应,且密度比煤油的大,则实验室中,少量的金属钠保存在盛有煤油的广口试剂瓶中,隔绝空气防止Na被氧化,故D正确;
故选D.
点评:本题考查钠的化学性质,为高频考点,把握Na与水、氧气及盐溶液的反应为解答的关键,注意性质与试剂保存的关系,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
下列化合物在水中的溶解度,排列次序正确的是( )
a.HOCH2CH2CH2OH b.CH3CH2CH2OH c.CH3CH2COOCH3 d.HOCH2CH(OH)CH2OH.
a.HOCH2CH2CH2OH b.CH3CH2CH2OH c.CH3CH2COOCH3 d.HOCH2CH(OH)CH2OH.
| A、d>a>b>c |
| B、c>d>a>b |
| C、d>b>c>a |
| D、c>d>b>a |
取四张湿润的蓝色石蕊试纸放在玻璃片上,然后按顺序分别滴加饱和的亚硫酸、98.3%的硫酸、新制氯水、浓氨水,四张试纸最后呈现的颜色是( )
| A、红、红、白、蓝 |
| B、红、黑、白、蓝 |
| C、白、白、白、蓝 |
| D、白、黑、白、蓝 |
下列各组物质中当总质量一定时,不论按何种比例混合,充分燃烧后,生成水的质量为一常量,且生成CO2质量也为一定值的是( )
| A、甲醛、乙醇、乙二醇 |
| B、苯、苯酚、苯乙烯 |
| C、乙炔、苯、苯乙烯 |
| D、甲烷、乙烷、乙烯 |
下列烷烃在光照下与氯气反应,生成二种一氯代烃的是( )
| A、CH3CH2CH2CH3 |
B、 |
C、 |
D、 |
某种氯原子的质量是a g 12C原子的质量是b g,NA用表示阿伏加德罗常数,下列说法正确的是
①氯元素的相对原子质量是
②mg该氯原子的物质的量是
mol
③该氯原子的摩尔质量是a NA g/mol
④ag该氯原子所含质子数是17NA( )
①氯元素的相对原子质量是
| 12a |
| b |
②mg该氯原子的物质的量是
| m |
| aNA |
③该氯原子的摩尔质量是a NA g/mol
④ag该氯原子所含质子数是17NA( )
| A、①③ | B、①④ | C、②③ | D、②④ |
下列方程式书写不正确的是( )
A、溴乙烷在氢氧化钠水溶液中加热,该反应的离子方程式:CH3CH2Br+OH-
| |||
B、实验室制乙烯的化学方程式:CH3CH2OH
| |||
C、苯酚钠溶液中通入少量CO2反应的离子方程式: +H2O+CO2→ +H2O+CO2→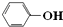 +HCO3- +HCO3- | |||
D、乙醛溶液与足量的银氨溶液共热的离子方程式:CH3CHO+2Ag(NH3)2++2OH-
|