题目内容
10.设NA表示阿伏加德罗常数值,下列说法正确的是( )| A. | 1 L 1mol/L CH3COONa溶液中存在NA个CH3COO-离子 | |
| B. | 在标准状况下,22.4LSO3含有3NA个氧原子 | |
| C. | 1 mol Cl2参加化学反应获得的电子数都是2NA | |
| D. | 1 mol NO2气体降温后颜色变浅,其所含的原子数仍为3NA |
分析 A、CH3COO-为弱酸根,在溶液中会水解;
B、标况下三氧化硫为固体;
C、根据氯气在反应中不一定得电子来分析;
D、NO2气体中存在平衡:2NO2?N2O4.
解答 解:A、CH3COO-为弱酸根,在溶液中会水解,故溶液中的醋酸根的个数小于NA个,故A错误;
B、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故B错误;
C、氯气在反应中不一定得电子,还可能失电子,故C错误;
D、NO2气体中存在平衡:2NO2?N2O4,正反应方向吸热,故降温后平衡右移,则颜色变浅,但整个过程中原子个数守恒,故所含的原子个数仍为3NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
1.下列说法正确的是( )
| A. | CH4的摩尔质量为16 | |
| B. | 1molH2O的质量为18g/mol | |
| C. | H2的气体摩尔体积约为22.4L | |
| D. | 在标准状况下,22.4 L由N2、N2O组成的混合气体的物质的量约1mol |
18.在反应4NH3+5O2═4NO+6H2O中,下列说法正确的是( )
| A. | NH3在反应中得到电子 | B. | O2在反应中失去电子 | ||
| C. | NO是反应的还原产物 | D. | 1mol氧化剂在反应中得到4mol电子 |
2.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0
T1温度下的部分实验数据为
下列说法不正确的是( )
T1温度下的部分实验数据为
| t/s | 0 | 500 | 1000 | 1500 |
| C(N2O5)mol/L | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500s内N2O5分解速率为2.96×10-3 mol/(L•s) | |
| B. | T1温度下的平衡常数为K1=125,1000s时转化率为50% | |
| C. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若K1<K2,则T1>T2 | |
| D. | 平衡后其他条件不变,将容器的体积压缩到原来的1/2,则再平衡时C(N2O5)>5.00mol/L |
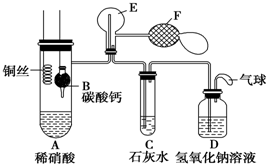 Ⅰ.乙组同学用如图装置来证明铜与稀硝酸反应产生一氧化氮,B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
Ⅰ.乙组同学用如图装置来证明铜与稀硝酸反应产生一氧化氮,B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.