题目内容
设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A、1molCl2参加反应转移电子数一定为2NA |
| B、1L0.1mol?L-1氨水含有0.1 NA个OH- |
| C、10LpH=1的硫酸溶液中含有的H+离子数为NA |
| D、常温常温下,2.24L丁烷分子所含的C-H键数为NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氯气发生氧化还原反应可以是自身氧化还原反应,也可以只做氧化剂;
B.一水合氨为弱电解质,只能部分电离;
C.依据pH=-lg[H+]计算氢离子浓度,依据n=CV计算氢离子的物质的量;
D.常温下Vm≠22.4L/mol.
B.一水合氨为弱电解质,只能部分电离;
C.依据pH=-lg[H+]计算氢离子浓度,依据n=CV计算氢离子的物质的量;
D.常温下Vm≠22.4L/mol.
解答:
解:A.1mol氯气参加氧化还原反应,自身氧化还原反应转移电子1mol,也可以只做氧化剂转移的电子数为2NA,故A错误;
B.一水合氨为弱电解质,只能部分电离,1L0.1mol?L-1氨水含有OH-个数小于0.1 NA,故B错误;
C.10L pH=1的硫酸溶液中氢离子浓度为0.1mol/L,1L溶液中含有0.1mol氢离子,含有的H+离子数为NA,故C正确;
D.常温下Vm≠22.4L/mol,2.24L丁烷分子的物质的量不是0.1mol,所含的C-H键数不为NA,故D错误;
故选:C.
B.一水合氨为弱电解质,只能部分电离,1L0.1mol?L-1氨水含有OH-个数小于0.1 NA,故B错误;
C.10L pH=1的硫酸溶液中氢离子浓度为0.1mol/L,1L溶液中含有0.1mol氢离子,含有的H+离子数为NA,故C正确;
D.常温下Vm≠22.4L/mol,2.24L丁烷分子的物质的量不是0.1mol,所含的C-H键数不为NA,故D错误;
故选:C.
点评:本题考查阿伏加德罗常数的有关计算和判断,注意标况下的气体摩尔体积使用条件,阿伏加德罗常数是高考的“热点”,解题时注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 天天向上课时同步训练系列答案
天天向上课时同步训练系列答案 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案
相关题目
关于如图所示的原电池,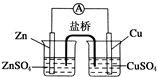 下列说法正确的是( )
下列说法正确的是( )
 下列说法正确的是( )
下列说法正确的是( )| A、盐桥中的阴离子向硫酸铜溶液中迁移 |
| B、锌电极发生还原反应,铜电极发生氧化反应 |
| C、铜电极上发生的电极反应是2H++e-→H2↑ |
| D、电子从锌电极通过检流计流向铜电极 |
下列关于Na和Na+的叙述中正确的是( )
| A、它们相差一个电子层 |
| B、它们都能与水反应 |
| C、钠原子、钠离子均为同一元素,因此是同种微粒 |
| D、灼烧时,它们的焰色反应都呈紫色 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(Al3+)=0.1mol/L的溶液中:Na+、K+、[Al(OH)4]-、SO42- |
| B、使酚酞呈红色的溶液中:K+、Ba2+、I-、NO3- |
| C、由水电离出的c(H+)=1×10-13mol/L的溶液中:Na+、HCO3-、Cl-、Br- |
| D、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
 图中的实验装置可用于制取乙炔.
图中的实验装置可用于制取乙炔.