题目内容
18.下列叙述中错误的是( )| A. | 原子半径 Na>Si>Cl | B. | 金属性 Na>Mg>Al | ||
| C. | 稳定性 SiH4<HCl<H2S | D. | 酸性 H3PO4<H2SO4<HClO4 |
分析 A.电子层数越多原子半径越大,电子层数相同时,核电荷数越多半径越小;
B.同周期元素从左到右元素的金属性逐渐减弱;
C.元素的非金属性越强,对应的氢化物越稳定;
D.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强.
解答 解:A.Na、Si、Cl核电荷数增多,半径减小,故A正确;
B.同周期元素从左到右元素的金属性逐渐减弱,金属性:Na>Mg>Al,故B正确;
C.非金属性:Cl>S>Si,元素的非金属性越强,对应的氢化物越稳定,则氢化物的稳定性:HCl>H2S>SiH4,故C错误;
D.非金属性:Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性H3PO4<H2SO4<HClO4,故D正确.
故选C.
点评 本题考查元素周期表与周期律的递变性,为高频考点,把握元素周期律、元素性质的比较等为解答的关键,学习中注重基础知识的积累,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.取少量MgO、Al2O3、SiO2、Fe2O3的混合粉末,加入过量盐酸,充分反应后过滤,得到沉淀X和滤液Y.下列叙述正确的是( )
| A. | 上述四种氧化物中,只有SiO2是酸性氧化物,它不溶于任何酸 | |
| B. | 向沉淀X中逐滴加入硝酸,沉淀慢慢溶解 | |
| C. | 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ | |
| D. | 溶液Y中加入过量氨水,所得沉淀为Fe(OH)3和Mg(OH)2 |
9.下列叙述正确的是( )
| A. | 元素处于最高价态,一定具有最强的氧化性 | |
| B. | 阳离子只有氧化性,阴离子只有还原性 | |
| C. | 还原剂失电子越多,还原性越强 | |
| D. | 在化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原 |
6.化学与人类生产、生活,社会可持续发展密切相关.下列说法正确的是( )
| A. | 蔬菜表面洒少许福尔马林,可保鲜和消毒 | |
| B. | 绿色食品就是不使用化肥农药,不含任何化学物质的食品 | |
| C. | 光催化水制氢比电解水制氢更节能环保 | |
| D. | 光化学烟雾不会引起呼吸道疾病 |
13.已知1~18号元素的离子aW3+、bX+、cY2-、dZ-都具有相同的电子层结构,下列关系正确的是( )
| A. | 质子数c>b | B. | 原子半径X<W | ||
| C. | 离子半径Y2-<Z- | D. | 离子的氧化性W3+>X+ |
3.下列溶液中NO${\;}_{3}^{-}$的物质的量浓度最大的是( )
| A. | 50 mL 1 mol•L-1的KNO3溶液 | B. | 50 mL 1 mol•L-1的Fe(NO3)3 | ||
| C. | 1 L 0.5 mol•L-1的Mg(NO3)2溶液 | D. | 1 L 0.5 mol•L-1的Ba(NO3)2溶液 |
10.下列有机物命名正确的是( )
| A. | 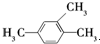 三甲苯 三甲苯 | B. | 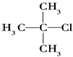 2甲基2氯丙烷 2甲基2氯丙烷 | C. | 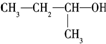 2甲基1丙醇 | D. | 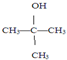 2-甲基-2丙醇 |
19.人们将连有四个不同基团的碳原子形象地称为手性碳原子,下列有机化合物分子中含有手性碳原子的是( )
| A. | CH3CH2CHO | B. | CH3CH=CHCH2CH3 | ||
| C. |  | D. |  |