题目内容
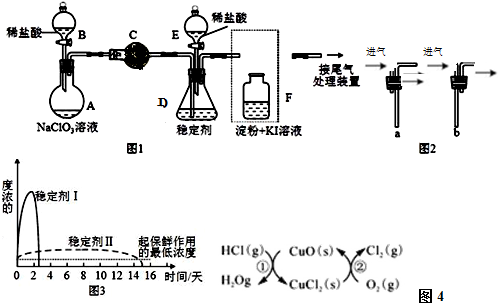
4.在反应“X+酸→化合物+H2O”中,反应条件已省去,X不可能是( )| A. | CuO | B. | NaCl | C. | SiO2 | D. |  |
分析 A.氧化铜为碱性氧化物,能够与酸反应生成盐和水;
B.氯化钠与酸反应为复分解反应;
C.二氧化硅与氢氟酸反应生成四氟化硅和水;
D.苯与浓硝酸发生取代反应生成硝基苯和水.
解答 解:A.CuO+2HCl=CuCl2+H2O,所以X可以为氧化铜,故A不选;
B.氯化钠与酸反应为复分解反应,不会生成水,所以X不能为氯化钠,故B选;
C.X为二氧化硅,则酸只能是氢氟酸,二者反应生成四氟化硅与水,X可以为二氧化硅,故C不选;
D.苯与浓硝酸发生取代反应生成硝基苯和水,所以X可以为苯,故D不选;
故选:B.
点评 本题考查物质推断,属于验证型题目,熟练掌握元素化合物与有机物的性质是关键,注意对基础知识的掌握,题目难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案 小学课时特训系列答案
小学课时特训系列答案
相关题目
19.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图1的Ⅰ、Ⅱ所示: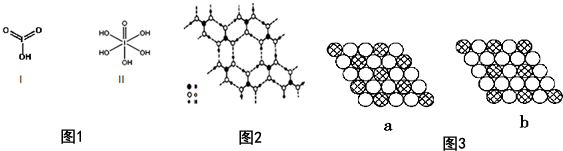
请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3B03分子间通过氢键相连(如图2).则1molH3BO3的晶体中有3 mol氢键.
硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2 O,它电离生成少量[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为共价键、配位键.
(6)如图所示的二维平面晶体示意图3中表示化学式为AX3的是b.
(1)卤族元素位于元素周期表的P区;溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF)2形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是碘(写出名称).
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |

请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3B03分子间通过氢键相连(如图2).则1molH3BO3的晶体中有3 mol氢键.
硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2 O,它电离生成少量[B(OH)4]一和H+,则[B(OH)4]一含有的化学键类型为共价键、配位键.
(6)如图所示的二维平面晶体示意图3中表示化学式为AX3的是b.
9.下列实验,温度计水银球不能放在液体中的是( )
| A. | 石油分馏实验 | B. | 乙醇脱水实验 | C. | 制溴苯 | D. | 苯的硝化实验 |
16.下列有机分子中,所有的原子不可能处于同一平面的是( )
| A. | CH2=CH-C≡N | B. | CH2=CH-CH=CH2 | C. |  | D. | 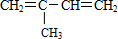 |
13.下列化合物不能通过化合反应获得的是( )
| A. | Fe(OH)3 | B. | CaSiO3 | C. | Al(OH)3 | D. | NaHCO3 |
14.下例物质发生反应后固体质量一定减少的是( )
| A. | FeCO3在空气中灼烧 | B. | 铝条插入冷的浓硫酸中 | ||
| C. | Na2O2敞放在空气中 | D. | 向Mg(OH)2悬浊液中加入FeCl3溶液 |

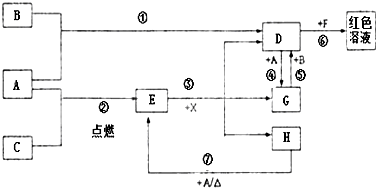 A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体.D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体.它们之间的转化如图所示(某些反应条件和部分反应产物已略去).
A、B、C为中学常见单质,其中一种为金属;通常情况下A为固体、B为黄绿色气体、C为无色气体.D、E、F、G、H、X均为化合物,其中X常温下是无色气体,其水溶液是一种无氧强酸溶液,E为黑色固体,H在常温下为液体.它们之间的转化如图所示(某些反应条件和部分反应产物已略去).