题目内容
13.已知X、Y、Z、W都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,而Z原子的最外层电子数是次外层的3倍,Y和Z可以形成两种以上气态化合物,W的族序数比X的族序数大1,则下列说法错误的是( )| A. | Y和Z以质量比7:16组成的共价化合物有两种 | |
| B. | X和Y、X和Z组成的常见化合物,稳定性前者大于后者 | |
| C. | X、Z、W简单离子的半径由大到小的顺序为:Z>W>X | |
| D. | X、Y、Z可以组成一种离子化合物,其中X、Y、Z元素原子个数比为4:2:3 |
分析 X、Y、Z、W都是短周期元素,它们的原子序数依次递增,X原子的电子层数与它的核外电子总数相等,X为H元素;而Z原子的最外层电子数是次外层的3倍,Z为O元素;Y和Z可以形成两种以上气态化合物,Y为N元素,W的族序数比X的族序数大1,W应为第三周期ⅡA族元素,以此来解答.
解答 解:由上述分析可知,X为H,Y为N,Z为O,W为Mg,
A.Y和Z以质量比7:16组成的共价化合物为NO2、N2O4,故A正确;
B.非金属性O>N,X和Y、X和Z组成的常见化合物,稳定性前者小于后者,故B错误;
C.具有相同电子排布的离子中原子序数大的离子半径小,电子层越多,离子半径越大,则X、Z、W简单离子的半径由大到小的顺序为:Z>W>X,故C正确;
D.X、Y、Z可以组成一种离子化合物为NH4NO3,X、Y、Z元素原子个数比为4:2:3,故D正确;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素化合物知识推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
3.设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 100mL0.4mol/L的甲酸中含甲酸的分子数为0.04NA | |
| B. | 在标准状态下,22.4L乙烷与乙烯的混合气体,含碳原子数为2NA | |
| C. | 18g水中含有的电子数为10NA | |
| D. | NA个23Na原子的质量为23g |
4.下列各组反应中,反应物的相对用量对产物组成无影响的是( )
| A. | 铁与稀硝酸 | B. | 硫化氢与氧气 | ||
| C. | 1,3-丁二烯与溴 | D. | 过氧化钠与二氧化碳 |
1.下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 用玻璃棒蘸取溶液X进行焰色反应实验 | 火焰呈黄色 | 溶液X中含有Na+ |
| B | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4 | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
| C | 在新生成的AgCl沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向饱和碳酸钠溶液中通入过量的CO2 | 溶液变浑浊 | 析出了Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
8.食用二氧化硫漂白过的食品,对人体的肝、肾脏等有严重损害.某科研小组设计实验检验二氧化硫的漂白性.回答下列问题:
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.
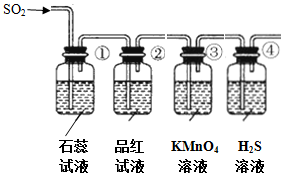
(2)根据上述实验,回答下列问题:
(3)用SO2漂白过的食品中一般残留有亚硫酸盐,科研小组设计了检验食品中是否含有亚硫酸盐的简单方法:将食品剪成碎末放入烧杯,加入适量的水,加热一会儿,冷却至室温,滴加盐酸和试剂A,观察液体的颜色变化既可.
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.
(一)二氧化硫的制备
实验室一般采用亚硫酸钠与硫酸(浓硫酸与水1:1混合)反应制取二氧化硫:

(1)欲收集一瓶干燥的二氧化硫,选择上图中的装置,其最佳连接顺序为:b→c→d→e→f→g(按气流方向,用小写字母表示).
(二)二氧化硫性质的检验
将上述收集到的SO2通入下列装置中,在一定温度下按图示装置进行实验.

(2)根据上述实验,回答下列问题:
| 序号 | 实验现象 | 解释原因 |
| ① | 石蕊试液变红 | 石蕊试液变红说明SO2是酸性气体 |
| ② | 品红试液褪色 | SO2具有漂白性 |
| ③ | KMnO4溶液颜色褪色 | 反应的离子方程式5SO2+2H2O+2MnO4-=2Mn2++5SO42-+4H+ |
| ④ | 溶液变浑浊,有黄色沉淀生成 | SO2+2H2S=3S↓+2H2O |
①加热的作用是加快反应速率(或加快食品的溶解),加热时间不能太长的原因是防止亚硫酸盐被氧化.
②试剂A是品红溶液.
18.短周期主族元素W、X、Y、Z原子序数依次增大,W是原子半径最小的短周期元素,W、Y同主族,X、Z同主族,且X、Z的原子序数之和是W、Y原子序数之和的2倍,下列叙述不正确的是( )
| A. | W和X形成的化合物可能含有非极性共价键 | |
| B. | X和Z形成的化合物常温下可能为固态 | |
| C. | W、X、Y、Z四种元素组成的化合物的水溶液可能呈酸性 | |
| D. | W、X、Y、Z四种元素两两之间均能形成化合物 |
2.实验室制备硝基苯时,经过配制混酸、硝化反应(50~60℃)、洗涤分液、干燥蒸馏等步骤,下列图示装置和原理能达到实验目的是( )
| A. | 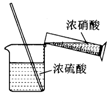 配制混酸 | B. | 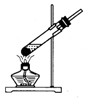 硝化反应 | C. |  分离硝基苯 | D. | 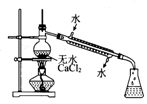 蒸馏硝基苯 |
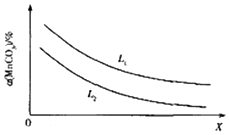 MnO2是常见的氧化剂、催化剂和活性电极材料.
MnO2是常见的氧化剂、催化剂和活性电极材料.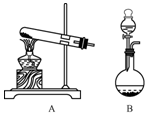 实验室制取氨气有几种方法.
实验室制取氨气有几种方法.