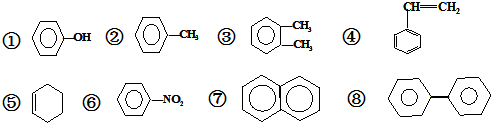
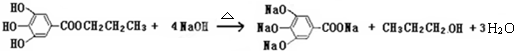题目内容
5.下列说法正确的是( )| A. | 离子化合物中只能含有离子键 | |
| B. | 共价化合物中可能含有离子键 | |
| C. | 含有离子键的化合物一定属于离子化合物 | |
| D. | 含共价键的化合物一定是共价化合物 |
分析 一般来说,活泼金属与非金属形成离子键,非金属之间形成共价键,含离子键的一定为离子化合物,离子化合物中可含共价键,以此来解答.
解答 解:A.离子化合物中可能含有离子键、共价键,如NaOH,故A错误;
B.共价化合物中一定不能含离子键,含离子键的一定为离子化合物,故不错哇;
C.含离子键的一定为离子化合物,故C正确;
D.含共价键的可能为离子化合物,如NaOH,故D错误;
故选C.
点评 本题考查离子化合物的结构,为高频考点,把握化学键的形成及判断的一般规律为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.25℃时某0.1mol/L的一元弱酸(用HA表示),未电离的弱酸分子(HA)的物质的量与电离生成的阴、阳离子总物质的量之比为4.5:1,则此溶液( )
| A. | 电离度α为10% | B. | α=20% | ||
| C. | pH=1 | D. | c(OH-)=1×10-12mol/L |
20.有以下说法:①氯原子和氯离子性质一样 ②+7价的氯只具有氧化性 ③氯原子比氯离子多一个电子 ④氯气具有氧化性,不具有还原性 ⑤氯原子比氯离子半径小 ⑥高氯酸是最高价含氧酸中酸性最强的,其中说法正确的是( )
| A. | ③⑤⑥ | B. | ①②③ | C. | ②⑤⑥ | D. | ④⑤⑥ |
10.已知同周期的X、Y、Z三种元素的最高价氧化物的水化物,其酸性由强到弱的顺序为 HZO4>H2YO4>H3XO4,判断下列叙述正确的是( )
| A. | 原子半径按X、Y、Z的顺序增大 | |
| B. | 单质的氧化性按X、Y、Z的顺序减弱 | |
| C. | 元素的非金属性按X、Y、Z的顺序增强 | |
| D. | 气态氢化物稳定性按X、Y、Z的顺序减弱 |
15.如表列出了A~R十二种元素在周期表中的位置:
请用相应的化学符号和化学用语回答下列问题:
(1)其中单质化学性质最不活泼的元素是Ar,最活泼的金属元素是K;
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是NaOH;其中J与F按原子个数1:1所成的化合物的电子式为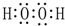 .
.
(3)A、B、C三种元素按离子半径由大到小的顺序排列为K+>Na+>Mg2+;
(4)元素G的气态氢化物比元素H的气态氢化物稳定(填“稳定”或“不稳定”).元素K和I的气态氢化物沸点较高的是NH3(填化学式).其原因是氨气分子之间存在氢键.
(5)元素G的单质溶于元素A的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的化学式为NaClO,该化合物中所含的化学键类型为离子键、共价键.
(6)元素B、C、D的简单阳离子的氧化性比较Al3+>Mg2+>Na+.(填离子符号)
(7)1g元素J的单质完全燃烧生成液态氧化物时放出的热量为142.9KJ,写出元素J的单质燃烧热的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1 .
| 主族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | J | |||||||
| 2 | E | K | F | |||||
| 3 | A | C | D | I | G | R | ||
| 4 | B | H |
(1)其中单质化学性质最不活泼的元素是Ar,最活泼的金属元素是K;
(2)A、C、D三种元素的氧化物对应的水化物,其中碱性最强的是NaOH;其中J与F按原子个数1:1所成的化合物的电子式为
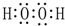 .
.(3)A、B、C三种元素按离子半径由大到小的顺序排列为K+>Na+>Mg2+;
(4)元素G的气态氢化物比元素H的气态氢化物稳定(填“稳定”或“不稳定”).元素K和I的气态氢化物沸点较高的是NH3(填化学式).其原因是氨气分子之间存在氢键.
(5)元素G的单质溶于元素A的最高价氧化物对应的水化物中,可生成具有漂白作用的一种盐,该盐的化学式为NaClO,该化合物中所含的化学键类型为离子键、共价键.
(6)元素B、C、D的简单阳离子的氧化性比较Al3+>Mg2+>Na+.(填离子符号)
(7)1g元素J的单质完全燃烧生成液态氧化物时放出的热量为142.9KJ,写出元素J的单质燃烧热的热化学方程式:H2(g)+$\frac{1}{2}$O2(g)=H2O(l)△H=-285.8kJ•mol-1 .

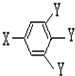 (其中:-X、-Y均为官能团)
(其中:-X、-Y均为官能团)