题目内容
(13分)实验室用下面装置测定FeO和Fe2O3固体混合物中Fe2O3的质量,D装置的硬质双通玻璃管中的固体物质是FeO和Fe2O3的混合物。

(1)为了安全,在点燃D处的酒精灯之前,在b出口处必须_________________________。
(2)装置B的作用是_ ______________;装置C中装的液体是_______,所起的作用是______。
(3)在气密性完好,并且进行了必要的安全操作后,点燃D处的酒精灯,在硬质双通玻璃管中发生反应的化学方程式是________________________________________。
(4)若FeO和Fe2O3固体混合物的质量为23.2 g,反应完全后U型管的质量增加7.2g,则混合物中Fe2O3的质量为___________g。
(5)U形管E右边又接连干燥管F的目的是____,若无干燥管F,测得Fe2O3的质量将_____(填“偏大”“偏小”或“无影响”)。
(6)若反应后得到的残留固体中还有少量FeO,测得的Fe2O3质量将______(填“偏大“偏小”或“无影响”)。
(1)检验氢气的纯度 (2)除去氢气中的氯化氢;浓硫酸;除水蒸气或干燥氢气
(3)3H2+Fe2O3 2Fe+3H2O,H2+FeO
2Fe+3H2O,H2+FeO Fe+H2O (4)16
Fe+H2O (4)16
(5)防止空气中水蒸气等气体进入E中;偏大 (6)偏下
【解析】
试题分析:(1)氢气是可燃性气体,为了安全,在点燃D处的酒精灯之前,在b出口处必须检验氢气的纯度。
(2)由于A中产生的H2中混有HCl和水蒸气,必须通过洗气逐一除去,防止干扰后续实验,所以B的作用是除去氢气中的氯化氢,C中盛放的是浓硫酸,用于干燥氢气;
(3)装置D中发生的是氧化亚铁、氧化铁与氢气的反应,反应方程式为:3H2+Fe2O3 2Fe+3H2O,H2+FeO
2Fe+3H2O,H2+FeO Fe+H2O;
Fe+H2O;
(4)U型管的质量增加的7.2g是水,物质的量是7.2g÷18g/mol=0.4mol。设FeO、Fe2O3物质的量分别为x、y,则:X+3Y=0.4
根据质量可列式:72X+160Y=23.2
解得Y=0.1,X=0.1,
所以氧化铁的质量为:160g/mol×0.1mol=16g。
(5)干燥管F的作用防空气中水蒸气对实验干扰,若无干燥管F,空气中的水蒸气被E吸收则所测生成水的质量增大,导致氧的含量增大,Fe2O3的质量将偏大。
(6)若反应后得到的残留固体中还有少量FeO,则测得的Fe2O3质量将导致生成水的质量减小,导致氧的含量减小,Fe2O3的质量将减小。
考点:考查测定FeO和Fe2O3固体混合物中Fe2O3质量的实验方案设计与评价等

(10分 )工业上用某矿渣(含有Cu2O、Al2O3、Fe2O3、SiO2)提取铜的操作流程如下:
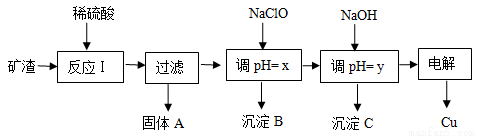
已知: Cu2O + 2H+ = Cu + Cu2+ + H2O
沉淀物 | Cu(OH)2 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 |
开始沉淀pH | 5.4 | 4.0 | 1.1 | 5.8 |
沉淀完全pH | 6.7 | 5.2 | 3.2 | 8.8 |
(1)反应I中如果Cu2O与Fe2O3之间恰好发生氧化还原反应,则反应的化学方程式为:___________________________________________________________________________
(2)用NaClO调pH=x是此工艺流程中的最佳选择。
①选择NaClO的理由是:____________________________________________________
②生成沉淀B的同时生成一种具有漂白作用的物质,写出该反应的离子方程式为:
_________________________________________________________________________
(3)如果某次测定pH=y的操作失误,将适量NaOH溶液滴加到0.02mol·L-1CuSO4溶液中,致使溶液中Cu2+浓度降至原来的百分之一,则溶液的pH为 ____。(已知常温下,Cu(OH)2的溶度积常数Ksp=2×10-20)
(4)电解初期阳极的电极反应式为________________________________
(10分)最近雾霾天气肆虐我国大部分地区,其中SO2是造成空气污染的主要原因,利用钠碱循环法可除去SO2。
(1)钠碱循环法中,吸收液为Na2SO3溶液,该反应的离子方程式是 。
(2)已知H2SO3的电离常数为K1=1.54×10-2,K2=1.024×10-7,H2CO3的电离常数为K1=4.30×10-7,K2=15.60×10-11,则下列微粒可以大量共存的是 (填序号)
A.CO32- 、HSO3- B.HSO3- 、HCO3- C.SO32- 、HCO3- D.HCO3-、H2SO3
(3)吸收液吸收SO2的过程中,pH随n(SO32-):n(HSO3-)变化关系如下表:
n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
pH | 8.2 | 7.2 | 6.2 |
①根据上表判断NaHSO3溶液显 性,试解释原因
②在NaHSO3溶液中离子浓度关系不正确的是
A.c(Na+)=2c(SO32-)+c(HSO3-)
B.c(H2SO3)+c(H+)= c(SO32-)+c(OH-)
C.c(Na+)> c(HSO3-)> c(H+)> c(SO32-)> c(OH-)
D.c(H+)+ c(Na+)=2c(SO32-)+c(HSO3-)+ c(OH-)
 N4H44++2 SO42-
N4H44++2 SO42-