题目内容
某温度时,浓度都为1mol/L的两种气体X2和Y2,在密闭容器中反应生成气体Z,4s后X2、Y2、Z的浓度分别是0.4mol/L,0.8mol/L,0.4mol/L,如Z用X、Y表示,则该化学方程式可表示为( )
| A、X2+2Y2═2XY2 |
| B、2X2+Y2═X2Y |
| C、3X2+Y2═2X3Y |
| D、X2+3Y2═2XY3 |
考点:化学平衡建立的过程
专题:化学平衡专题
分析:计算各物质的浓度变化量,利用浓度变化量之比等于化学计量数之比,据此确定各物质的化学计量数,再利用原子守恒用X、Y表示Z的组成,据此书写方程式.
解答:
解:4s后,△c(X2)=1mol?L-1-0.4mol?L-1=0.6mol?L-1,
△c(Y2)=1mol?L-1-0.8mol?L-1=0.2mol?L-1,
△c(Z)=0.4mol?L-1,
则X2、Y2、Z的化学计量数之比为=0.6mol?L-1:0.2mol?L-1:0.4mol?L-1=3:1:2,
故反应为3X2+Y2═2Z,根据原子守恒可知,Z为X3Y,
故反应可以表示为:3X2+Y2═2X3Y,
故选:C.
△c(Y2)=1mol?L-1-0.8mol?L-1=0.2mol?L-1,
△c(Z)=0.4mol?L-1,
则X2、Y2、Z的化学计量数之比为=0.6mol?L-1:0.2mol?L-1:0.4mol?L-1=3:1:2,
故反应为3X2+Y2═2Z,根据原子守恒可知,Z为X3Y,
故反应可以表示为:3X2+Y2═2X3Y,
故选:C.
点评:本题考查化学反应速率的有关计算,难度不大,根据物质的量浓度变化量之比等于化学计量数之比确定各物质的化学计量数是关键.

练习册系列答案
相关题目
下列说法中正确的是( )
| A、可以利用紫色石蕊试液一次性把NaOH 溶液、稀硫酸、NaCl溶液鉴别出来 |
| B、可以按溶解、过滤、蒸发的操作顺序将硝酸钾和硝酸钠它们分离出来 |
| C、用氢气还原氧化铜实验中,先加热再通入氢气 |
| D、稀释浓硫酸时,先在烧杯里倒入浓硫酸,再小心倒入水并不断搅拌 |
我国北方地区雾霾天气频发,PM2.5是形成雾霾的罪魁祸首.PM2.5主要是指( )
| A、二氧化碳 | B、一氧化碳 |
| C、二氧化硫 | D、可吸入颗粒物 |
检验烧碱(NaOH)中是否混有纯碱(Na2CO3),以下方法可行的是( )
| A、加热后观察是否有气体产生 |
| B、溶于水后滴加稀氯化钙溶液观察是否有沉淀产生 |
| C、溶于水后检验溶液是否显碱性 |
| D、溶于水后通入CO2观察是否有NaHCO3产生 |
下列表达正确的是( )
A、TNT |
B、石炭酸 |
| C、聚丙烯的链节:CH3CH=CH2 |
| D、软脂酸:C17H33COOH |
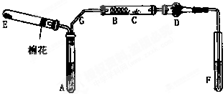 如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.
如图是某化学兴趣小组设计的乙醇催化氧化的实验装置(图中加热仪器、铁架台、试管夹均未画出).图中A处为无水乙醇(沸点78℃),B处为绕成螺旋状的细铜丝或银丝,C处为无水CuSO4粉末,D处为碱石灰,F处为新制的碱性Cu(OH)2悬浊液.