题目内容
下列反应中,氧化剂与还原剂的物质的量之比为2:1的是( )
| A、Zn+2HCl=ZnCl2+H2↑ |
| B、Cu+2 H2SO4(浓)=CuSO4+SO2↑+2H2O |
| C、3S+6NaOH=2Na2S+Na2SO3+3H2O |
| D、2Na+Cl2=2NaCl |
考点:氧化还原反应
专题:氧化还原反应专题
分析:根据元素的化合价的变化,判断氧化剂和还原剂,结合物质的量的关系从化合价的角度分析.
解答:
解:A.反应中HCl为氧化剂,Zn为还原剂,二者物质的量之比为2:1,故A正确;
B.H2SO4反应中为氧化剂,Cu为氧化剂,由反应可知,H2SO4并不都表现氧化性,氧化剂和还原剂物质的量之比为1:1,故B错误;
C.只有S元素化合价发生变化,如3molS参加反应,生成2molNa2S,1molNa2SO3,氧化剂与还原剂的物质的量之比为2:1,故C正确;
D.氧化剂为Cl2,还原剂为Na,氧化剂与还原剂的物质的量之比为1:2,故D错误.
故选AC.
B.H2SO4反应中为氧化剂,Cu为氧化剂,由反应可知,H2SO4并不都表现氧化性,氧化剂和还原剂物质的量之比为1:1,故B错误;
C.只有S元素化合价发生变化,如3molS参加反应,生成2molNa2S,1molNa2SO3,氧化剂与还原剂的物质的量之比为2:1,故C正确;
D.氧化剂为Cl2,还原剂为Na,氧化剂与还原剂的物质的量之比为1:2,故D错误.
故选AC.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化剂、还原剂判断及物质的量关系的考查,题目难度不大.

练习册系列答案
相关题目
已知有如下平衡体系:3A(g)+B(g)?2C(g),现等物质的量的投料反应物A、B于恒温恒容体系I和恒温、恒压体系Ⅱ中,达平衡时体系I中A的物质的量浓度为M,体系Ⅱ中A的物质的量浓度为m,则M与m的关系为( )
| A、M=m | B、M>m |
| C、M<m | D、以上情况都有可能 |
久置的氯水中不含有的微粒是( )
| A、Cl- |
| B、HClO |
| C、H+ |
| D、H2O |
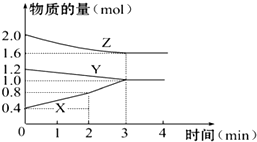 某温度时,在容积为3L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析正确的是( )
某温度时,在容积为3L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析正确的是( )| A、该反应的化学方程式为Y+2Z=3X |
| B、反应开始至2 min时,X的逆反应速率要大于正反应速率 |
| C、该反应是由正、逆反应同时开始的 |
| D、若增加Y的用量,化学反应速率不变化,则Y一定为固态 |
下列有关说法不正确的是( )
| A、C3H8中碳原子都采用的是sp3杂化 |
| B、O2、CO2、N2都是非极性分子 |
| C、酸性:H2CO3<H3PO4<H2SO4<HClO |
D、CO的一种等电子体为NO+,它的电子式为 |
常温下,下列各组离子一定能大量共存的是( )
| A、甲基橙变红的溶液中:Cu2+、Al3+、NO3-、I- |
| B、氢氧化铁胶体中:H+、K+、SO42-、Br- |
| C、含有大量的CO32-溶液中:NH4+、Na+、SO42-、Cl- |
| D、c(Al3+)=0.1 mol?L-1的溶液中:Na+、Cl-、HCO3-、SO42- |
下列说法正确的是( )
| A、Li是最活泼金属,F是最活泼非金属 |
| B、元素周期表有7个主族,7个副族,1个0族,1个Ⅷ族,共16纵行 |
| C、X2+的核外电子数目为18,则X在第四周期第ⅡA族 |
| D、Mg(OH)2碱性比Ca(OH)2强 |
下列各组离子中,能大量共存的是( )
| A、K+、Cl-、CO32-、Ca2+ |
| B、H+、Fe2+、NO3-、Na+ |
| C、NH4+、SO42-、K+、OH- |
| D、Na+、NH4+、Cl-、NO3- |