题目内容
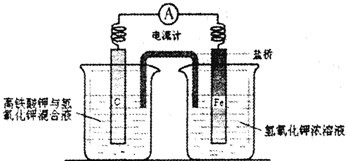
 如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段后测得导线上通过了0.02mole-.若不考虑溶液体积变化,下列叙述正确的是( )
如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段后测得导线上通过了0.02mole-.若不考虑溶液体积变化,下列叙述正确的是( )分析:(2)为原电池,锌为负极,发生氧化反应,电极方程式为Zn-2e-=Zn2+,铜为正极,发生还原反应,电极方程式为2H++2e-=H2↑,(1)为电解池,阳极反应为4OH--4e-=2H2O+O2↑,阴极反应为Cu2++2e-=Cu,为电解硫酸铜的反应,以此解答该题.
解答:解:A.相同条件下,如转移0.02mol电子,则(2)正极发生2H++2e-=H2↑,生成0.01molH2,(1)阳极发生4OH--4e-=2H2O+O2↑,生成0.005molO2,故A错误;
B.(1)pH增大,(2)溶液的pH值减小,故B错误;
C.(1)为电解池,阳极反应为4OH--4e-=2H2O+O2↑,故C正确;
D.工作一段后测得导线上通过了0.02mole-,(1)中阴极反应为Cu2++2e-=Cu,析出0.01molCu,质量为0.64g,故D正确.
故选CD.
B.(1)pH增大,(2)溶液的pH值减小,故B错误;
C.(1)为电解池,阳极反应为4OH--4e-=2H2O+O2↑,故C正确;
D.工作一段后测得导线上通过了0.02mole-,(1)中阴极反应为Cu2++2e-=Cu,析出0.01molCu,质量为0.64g,故D正确.
故选CD.
点评:本题考查原电池和电解池知识,侧重于学生的分析能力和电化学知识的综合考查,为高考常见题型和高频考点,注意根据电极方程式的书写和电池种类的判断,难度不大.

练习册系列答案
相关题目
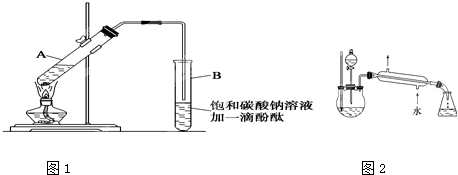
 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O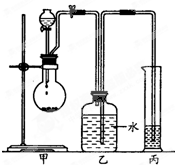 某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.
某化学小组探究液体有机物样品A(C3H8O2)的结构,进行如下实验.