题目内容
某学生用0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,其操作可分解为如下几步:
(A)移取20.OOmL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或O刻度以下,记下读数
(F)把锥形瓶放在滴定管下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空;
(1)正确操作的顺序是(用序号字母填写) .
(2)上述(B)操作的目的是 .
(3)判断到达滴定终点的实验现象 .
(4)下列情况使结果偏高的是 .
①碱式滴定管用水洗后直接装液体进行滴定;
②酸式滴定管水洗后,就用来量取待测盐酸;
③锥形瓶用蒸馏水洗涤后,又用待测盐酸润洗;
④将待测酸液溅到锥形瓶外;
⑤碱液在滴定时滴到锥形瓶外;
⑥若称取含少量NaOH的KOH固体配制标准溶液并用来滴定上述盐酸;
⑦滴定前,碱式滴定管有气泡,滴定后消失;
⑧记录标准碱液起始体积时,仰视读数,终点时俯视.
(A)移取20.OOmL待测的盐酸溶液注入洁净的锥形瓶,并加入2-3滴酚酞
(B)用标准溶液润洗滴定管2-3次
(C)把盛有标准溶液的碱式滴定管固定好,调节液面使滴定管尖嘴充满溶液
(D)取标准KOH溶液注入碱式滴定管至0刻度以上2-3cm
(E)调节液面至0或O刻度以下,记下读数
(F)把锥形瓶放在滴定管下面,用标准KOH溶液滴定至终点,记下滴定管液面的刻度
完成以下填空;
(1)正确操作的顺序是(用序号字母填写)
(2)上述(B)操作的目的是
(3)判断到达滴定终点的实验现象
(4)下列情况使结果偏高的是
①碱式滴定管用水洗后直接装液体进行滴定;
②酸式滴定管水洗后,就用来量取待测盐酸;
③锥形瓶用蒸馏水洗涤后,又用待测盐酸润洗;
④将待测酸液溅到锥形瓶外;
⑤碱液在滴定时滴到锥形瓶外;
⑥若称取含少量NaOH的KOH固体配制标准溶液并用来滴定上述盐酸;
⑦滴定前,碱式滴定管有气泡,滴定后消失;
⑧记录标准碱液起始体积时,仰视读数,终点时俯视.
考点:中和滴定
专题:实验题
分析:(1)根据中和滴定有检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等操作;
(2)滴定管在装液时,为了防止溶液被稀释,需用待装液润洗;
(3)如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(4)根据c(待测)=
分析,由错误操作引起VV(待测)的变化分析产生的误差.
(2)滴定管在装液时,为了防止溶液被稀释,需用待装液润洗;
(3)如溶液颜色变化且半分钟内不变色,可说明达到滴定终点;
(4)根据c(待测)=
| c(标准)×V(标准) |
| V(待测) |
解答:
解:(1)中和滴定按照检漏、洗涤、润洗、装液、取待测液并加指示剂、滴定等顺序操作,则正确的顺序为BDCEAF,
故答案为:BDCEAF;
(2)上述(B)操作的目的是防止将标准液稀释,故答案为:防止将标准液稀释;
(3)0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,酚酞在盐酸中为无色,到达终点时变为浅红色,则锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色,可说明达到滴定终点,
故答案为:锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色;
(4)①碱式滴定管用水洗后直接装液体进行滴定,KOH溶液被稀释,所用KOH溶液体积偏大,所测盐酸浓度偏高,故①正确;
②酸式滴定管水洗后,就用来量取待测盐酸,盐酸被稀释,待测液的物质的量偏小,所用KOH溶液体积偏小,所测盐酸浓度偏小,故②错误;
③锥形瓶用蒸馏水洗涤后,又用待测盐酸润洗,待测液的物质的量偏大,所用KOH溶液体积偏大,所测盐酸浓度偏高,故③正确;
④将待测酸液溅到锥形瓶外,待测液的物质的量偏小,所用KOH溶液体积偏小,所测盐酸浓度偏小,故④错误;
⑤碱液在滴定时滴到锥形瓶外,所用KOH溶液体积偏大,所测盐酸浓度偏大,故⑤正确;
⑥同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾的物质的量,所以若称取含少量NaOH的KOH固体配制标准溶液,标准溶液中氢氧根离子的浓度偏大,滴定时造成V(标)偏小,所测盐酸浓度偏小,故⑥错误;
⑦滴定前,碱式滴定管有气泡,滴定后消失,所用KOH溶液体积偏大,所测盐酸浓度偏大,故⑦正确;
⑧记录标准碱液起始体积时,仰视读数,终点时俯视,所用KOH溶液体积偏小,所测盐酸浓度偏小,故⑧错误;
故答案为:①③⑤⑦.
故答案为:BDCEAF;
(2)上述(B)操作的目的是防止将标准液稀释,故答案为:防止将标准液稀释;
(3)0.1mol/L KOH溶液滴定未知浓度的盐酸溶液,酚酞在盐酸中为无色,到达终点时变为浅红色,则锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色,可说明达到滴定终点,
故答案为:锥形瓶中溶液的颜色由无色变浅红且保持半分钟内不褪色;
(4)①碱式滴定管用水洗后直接装液体进行滴定,KOH溶液被稀释,所用KOH溶液体积偏大,所测盐酸浓度偏高,故①正确;
②酸式滴定管水洗后,就用来量取待测盐酸,盐酸被稀释,待测液的物质的量偏小,所用KOH溶液体积偏小,所测盐酸浓度偏小,故②错误;
③锥形瓶用蒸馏水洗涤后,又用待测盐酸润洗,待测液的物质的量偏大,所用KOH溶液体积偏大,所测盐酸浓度偏高,故③正确;
④将待测酸液溅到锥形瓶外,待测液的物质的量偏小,所用KOH溶液体积偏小,所测盐酸浓度偏小,故④错误;
⑤碱液在滴定时滴到锥形瓶外,所用KOH溶液体积偏大,所测盐酸浓度偏大,故⑤正确;
⑥同质量的氢氧化钠和氢氧化钾,氢氧化钠的物质的量大于氢氧化钾的物质的量,所以若称取含少量NaOH的KOH固体配制标准溶液,标准溶液中氢氧根离子的浓度偏大,滴定时造成V(标)偏小,所测盐酸浓度偏小,故⑥错误;
⑦滴定前,碱式滴定管有气泡,滴定后消失,所用KOH溶液体积偏大,所测盐酸浓度偏大,故⑦正确;
⑧记录标准碱液起始体积时,仰视读数,终点时俯视,所用KOH溶液体积偏小,所测盐酸浓度偏小,故⑧错误;
故答案为:①③⑤⑦.
点评:本题考查酸碱中和滴定实验,题目难度中等,注意把握实验的原理、步骤、方法以及注意事项,把握实验基本操作,侧重于考查学生的实验能力和分析能力.

练习册系列答案
相关题目
某研究小组利用“钯催化交叉偶联反应”合成了有机物丙,合成路线如图:

下列分析判断正确的是( )

下列分析判断正确的是( )
| A、分离提纯有机物丙易在NaOH热溶液中进行 |
| B、利用NaOH溶液、AgNO3溶液即可确定有机物甲中含有溴元素 |
| C、可用酸性KMnO4溶液鉴别有机物丙中是否混有有机物乙 |
| D、PbCl2的作用是提高反应物的活性和产量 |
下列说法正确的是( )
| A、HCO3-在水溶液中只电离,不水解 |
| B、硝酸钠溶液水解之后呈中性 |
| C、可溶性的铝盐都能发生水解反应 |
| D、可溶性的钾盐都不能发生水解反应 |
某些金属遇到某些酸会形成一层致密的“膜”,使金属不致溶解,以下不属于这种情况的是( )
| A、铝与浓硫酸 |
| B、铁与浓硝酸 |
| C、铜与稀硫酸 |
| D、铅与氢氟酸 |
汽车的安全气囊内有叠氮酸钠(NaN3)和硝酸钾,当汽车发生碰撞时引发如下反应10NaN3+2KNO3═K2O+5Na2O+16N2,则氧化剂和还原剂的物质的量之比为( )
| A、1:5 | B、5:1 |
| C、1:1 | D、3:5 |
樱桃是一种抗氧化的水果,对人体有很大的益处,樱桃中含有一种羟基酸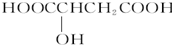 具有健脾作用.下列有关说法正确的是( )
具有健脾作用.下列有关说法正确的是( )
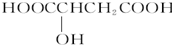 具有健脾作用.下列有关说法正确的是( )
具有健脾作用.下列有关说法正确的是( )| A、该羟基酸含有3种官能团 |
| B、通常条件下,该羟基酸可以发生取代、氧化和加成反应 |
| C、该羟基酸可以在Cu的催化下被O2氧化成醛 |
| D、含1mol该羟基酸的溶液可与含2mol氢氧化钠的溶液恰好完全反应 |
 I.有机物A为绿色荧光蛋白在一定条件下水解的最终产物之一,结构简式如图.
I.有机物A为绿色荧光蛋白在一定条件下水解的最终产物之一,结构简式如图.


 .请写出以
.请写出以  、CH3CH2CH2COCl为原料制备
、CH3CH2CH2COCl为原料制备  的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).