题目内容
9.两种不同浓度的Na0H溶液,c(H+)分别为1×10-14mol•L-1和1×10-10mol•L-1,等体积混合后,所得溶液中的c(H+)是( )| A. | 1×(10-14+10-10)mol•L-1 | B. | $\frac{1×{(10}^{-14}{+10}^{-10})}{2}$mol•L-1 | ||
| C. | 2×10-10mol•L-1 | D. | 2×10-14mol•L-1 |
分析 先根据pH分别计算出氢氧化钠溶液中氢氧根离子浓度,然后计算出混合液中氢氧根离子总浓度,再根据水的离子积计算出混合后溶液中氢离子浓度.
解答 解:c(H+)为1×10-14 mol•L-1的NaOH溶液中氢氧根离子浓度为1mol/L,
c(H+)为1×10-10 mol•L-1的NaOH溶液中氢氧根离子浓度为10-4mol/L,
等体积混合后,溶液中氢氧根离子浓度为:$\frac{1}{2}$(1mol/L+10-4mol/L)≈0.5mol/L,
则混合液中氢离子浓度为:c(H+)=$\frac{1×1{0}^{-14}}{0.5}$mol/L=2.0×10-14mol/L,
故选D.
点评 本题以物质的量浓度计算为载体,考查溶液pH的有关计算,混合后溶液呈碱性时,要先计算混合后溶液中氢氧根离子浓度,再结合水的离子积计算氢离子浓度.

练习册系列答案
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案
相关题目
17.乳酸的一种合成方法如图所示,下列说法正确的是( )

| A. | 步骤①、②分别是加成反应、取代反应 | B. | 蛋白质水解也可生成乳酸 | ||
| C. | 丙酸烃基上的二氯代物有2种 | D. | 乳酸与丙烯完全燃烧的产物相同 |
4.下列是元素周期表的前三周期中的部分元素
(1)表中所标出的元素当中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ne;
(2)K和Mg两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:KOH大于Mg(OH)2 (大于/小于);
(3)Si元素位于元素周期表的第三周期第ⅣA族,它的最高价氧化物的化学式是SiO2;其最高价氧化物对应水化物的化学式为H2SiO3.
(4)已知①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl.据此推断,活泼性比较:O2小于Cl2 (大于/小于);
另由③Cl2+2NaBr=Br2+2NaCl,可推断氧化性比较:Cl2大于 Br2 (大于/小于).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | Li | C | N | O | F | Ne | ||
| 三 | Na | Mg | S | Cl | ||||
| 四 | K | Ca | Br |
(2)K和Mg两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:KOH大于Mg(OH)2 (大于/小于);
(3)Si元素位于元素周期表的第三周期第ⅣA族,它的最高价氧化物的化学式是SiO2;其最高价氧化物对应水化物的化学式为H2SiO3.
(4)已知①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl.据此推断,活泼性比较:O2小于Cl2 (大于/小于);
另由③Cl2+2NaBr=Br2+2NaCl,可推断氧化性比较:Cl2大于 Br2 (大于/小于).
2.下列说法错误的是( )
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、H+和H2是氢元素的五种不同粒子 | |
| B. | 石墨和金刚石互为同位素,化学性质相似 | |
| C. | ${\;}_{1}^{1}$H和 ${\;}_{1}^{2}$H是不同的核素 | |
| D. | 12C和 14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
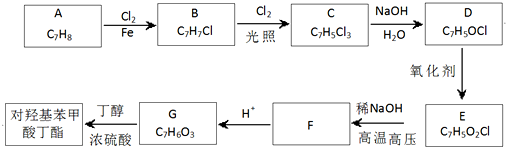
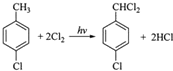 ;
; ;
; ;
;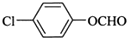 (写结构简式).
(写结构简式).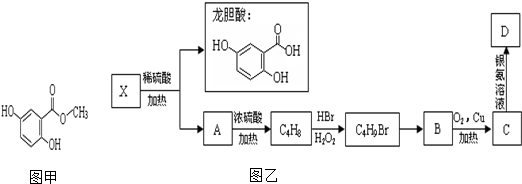
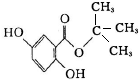 .
. .
. ;MgF2
;MgF2 .
.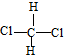 和
和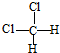
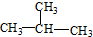

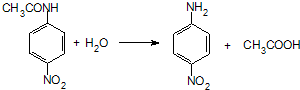
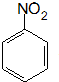 、
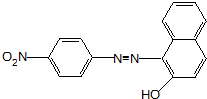
、
 (写出符合要求的所有结构简式)
(写出符合要求的所有结构简式) .
.