题目内容
有A、B、C、D、E、F、G、H、I九种常见物质,它们的转化关系(反应条件未注明)如图所示.其中B、C、D为单质,常温下D为固态,B、C、E、G为气态,F为淡黄色粉末,I的焰色反应为黄色.
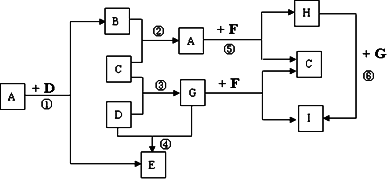
请回答:
(1)写出F的电子式________,其化学键类型有________.
(2)写出反应⑤的化学方程式________.
(3)I的是溶液呈________性(填酸性、中性或碱性),原因(用离子反应方程式表示)________.
(4)B、C单质已被应用于字宙飞船的燃料电池中,如图所示,两个电极均由多孔性碳构成,通入的两种单质由孔隙逸出并在电极表面放电.b是电池的________极;a电极上的电极反应是________.

(5)在①、②、③、④、⑤五个反应中,ΔH>0的反应是________(填序号).
(6)在标准状况下,若将11.2 L气体G通入350 mL 2 mol/L的H溶液中,反应后溶液中离子浓度由大到小的顺序是________.
解析:
|
答案:(1) (2)2Na2O2+2H2O=4NaOH+O2↑ (4)正极 H2+2OH--2e-=2H2O (5)①④ (6)c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) 解析:(1)由F为淡黄色粉末、I的焰色反应为黄色,可推知F为Na2O2,又因为G为气态、C为单质,可推知G为CO2、C为O2,I为Na2CO3;又因为A和F(Na2O2)产生O2,可推知A为H2O;又因B和O2生成水,且B为单质,故B为H2;又因为A(H2O)和D反应生成H2,且D为单质,可推知D为碳;D(碳)和CO2反应生成E,故E为CO. (5)反应①为C+H2O=CO+H2,反应④为CO2+C=2CO,它们都是吸热反应,其他反应为放热反应. (6)0.5 mol通入0.7 mol NaOH的溶液中,生成0.2 mol Na2CO3、0.3 mol NaHCO3,故在它们的溶液中离子浓度大小顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+). |






