题目内容
溴被称为“海洋元素”.已知Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.实验室模拟从海水中提取溴的主要步骤为:

步骤1:将海水蒸发浓缩除去粗盐;
步骤2:将除去粗盐后的母液酸化后,通入适量的氯气,使Br-转化为Br2;
步骤3:向步骤2所得的水溶液中通入热空气或水蒸气,将溴单质吹入盛有二氧化硫水溶液的容器中;
步骤4:再向该容器中通入适量的氯气,使Br-转化为Br2;
步骤5:用四氯化碳萃取溴单质,经分液、蒸馏得粗溴.
(1)步骤3中的反应的离子方程式________.
(2)步骤2中已经制得了溴,还要进行步骤3和步骤4的原因是________.
(3)步骤5中萃取和分液所需要的主要玻璃仪器为________.
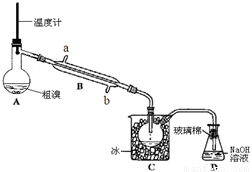
(4)用如上图所示的实验装置可精制粗溴.
①反应过程中需要对A容器加热,加热的方法是________.图中冷却水应从B的________口进入
(填“a”或“b”).②C
中加冰的目的是________.
答案:

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案
相关题目