题目内容
(16分)
(1)合成氨反应反应N2(g)+3H2(g)2NH3(g),若在恒温、恒压条件下向平衡体系中通入氩气,平衡 移动(填“向左”“向右”或“不”);使用催化剂 反应的ΔH(填“增大”“减小”或“不改变”)。
(2)已知:N2H4(g)+O2(g)=N2(g)+2H2O(g);△H=-543kJ·mol-1
H2(g)+
F2(g)=HF(g);△H=-269kJ·mol-1
H2(g)+O2(g)=H2O(g);△H=-242kJ·mol-1
则反应 N2H4(g)+2F2(g)=N2(g)+4HF(g) 的H=_____________ kJ·mol-1。
(3)已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.2×10-20。在25℃下,向浓度均为0.1 mol·L-1的MgCL2和CuCl2混合溶液中逐滴加入氨水,先生成__________沉淀(填化学式),生成该沉淀的离子方程式为______。
(4)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显_____________性(填“酸”“碱”或“中”);用含a的代数式表示此时溶液中NH3·H2O的物质的量浓度__________ mol·L-1。(说明:溶液的体积可以直接相加)
(1)向左 (2分) 不改变(2分)
(2)-1135(kJ·mol-1 ) (2分)
(3)Cu(OH)2 (2分) Cu2++2NH3·H2O=Cu(OH)2 ↓+2NH4+(3分)
(4)中(2分); mol·L-1(3分)
解析:

练习册系列答案
相关题目
合成氨反应为:N2(g)+3H2(g)?2NH3(g).图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线.图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响.

下列说法正确的是( )

下列说法正确的是( )
| A、该反应为自发反应,由图1可得加入适当的催化剂,E和△H都减小 | B、图2中0~10min内该反应的平均速率v(H2)=0.045mol?L-1?min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为d | C、图3中a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是b点 | D、图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1>T2,K1>K2 |
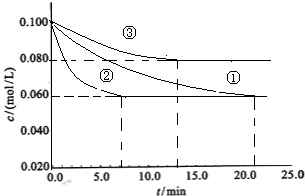
 2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在一定的温度下此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。