题目内容
将反应4(NH4)2SO4→N2↑+6NH3↑+3SO2↑+SO3↑+7H2O的产物气体通入BaCl2溶液,下列判断正确的是( )
| A、无沉淀生成 | B、肯定没有BaSO3生成 | C、得到的沉淀是纯净物 | D、得到的沉淀是BaSO4和BaSO3组成的混合物 |
分析:根据反应生成的产物量和性质分析,二氧化硫溶于水和水反应生成亚硫酸,三氧化硫溶于水和水反应生成硫酸,氨气溶于水生成一水合氨,硫酸和氯化钡反应生成硫酸钡沉淀,亚硫酸和氨水反应生成亚硫酸铵,所以通入氯化钡溶液中,关键分解反应生成的气体物质的量进行计算分析判断,生成沉淀有亚硫酸钡和硫酸钡.
解答:解:反应后的混合气体通入到BaCL2溶液中发生的是复分解反应:SO2+H2O+2NH3=(NH4)2SO3 ;(NH4)2SO3+BaCl2=BaSO3↓+2NH4Cl;SO3+H2O+2NH3 =(NH4)2SO4;(NH4)2SO4+BaCl2=BaSO4↓+2NH4Cl(先反应).依据反应定量关系,结合分解生成的气体物质的量可知,1mol三氧化硫转化为1mol硫酸铵消耗氨气2mol,则还会剩余4mol氨气,即此时4mol氨水会和2mol二氧化硫反应生成2mol亚硫酸铵,1mol硫酸铵对应得到的沉淀为1mol硫酸钡,2mol亚硫酸铵对应得到2mol亚硫酸钡,剩余1mol二氧化硫和2mol亚硫酸钡反应生成1mol亚硫酸氢钡,剩余1mol亚硫酸钡,最后得到沉淀为1mol硫酸钡,1mol亚硫酸钡,因此得到沉淀为BaSO3和BaSO4.
故选D.
故选D.
点评:本题考查了物质反应的定量计算及物质性质的综合应用,关键是分析反应过程反应判断沉淀生成的实质,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目

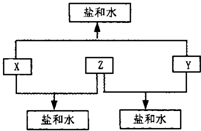 (2010?潍坊一模)已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题.
(2010?潍坊一模)已知:A、B、C、D四种短周期元素,A与D的原子序数之和等于B与C的原子序数之和,由D元素组成的单质在通常状况下呈黄绿色,B、C、D三种元素位于同一周期,A、B、C三种元素的最高价氧化物对应的水化物分别为X、Y、Z,且存在如下转化关系,试推断回答下列问题.