题目内容
下列电离方程式中正确的是( )
| A、NH3?H2O=NH4++OH- |
| B、H2SO4=H2++SO42- |
| C、NaOH=Na++H++O2- |
| D、NaHCO3=Na++HCO3- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.弱电解质不完全电离,用可逆号;
B.硫酸为强电解质,完全电离生成氢离子和硫酸根离子;
C.氢氧化钠为强电解质,完全电离生成氢氧根离子和钠离子;
D.NaHCO3为强电解质,完全电离生成碳酸氢根离子和钠离子;
B.硫酸为强电解质,完全电离生成氢离子和硫酸根离子;
C.氢氧化钠为强电解质,完全电离生成氢氧根离子和钠离子;
D.NaHCO3为强电解质,完全电离生成碳酸氢根离子和钠离子;
解答:
解:A.一水合氨为弱电解质,电离方程式为:NH3?H2O NH4++OH-,故A错误;
B.硫酸为强电解质,电离方程式为:H2SO4=2H++SO42-,故B错误;
C.NaOH为强电解质,电离方程式为:NaOH=Na++OH-,故C错误;
D.NaHCO3为强电解质,电离方程式为:NaHCO3=Na++HCO3-,故D正确;
故选:D.
B.硫酸为强电解质,电离方程式为:H2SO4=2H++SO42-,故B错误;
C.NaOH为强电解质,电离方程式为:NaOH=Na++OH-,故C错误;
D.NaHCO3为强电解质,电离方程式为:NaHCO3=Na++HCO3-,故D正确;
故选:D.
点评:本题考查了电解质电离方程式的书写,是高考的热点,明确电解质的强弱、掌握正确书写电离方程式的方法是解题关键,题目难度不大.

练习册系列答案
相关题目
下列有关实验室一般事故的预防和处理方法正确的是( )
| A、燃着的酒精灯打翻失火,应用黄沙扑灭 |
| B、少量浓硫酸溅到手,马上用大量水冲洗,再涂上稀硼酸 |
| C、金属钠着火,用CO2灭火 |
| D、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
下列关于臭氧性质的叙述中,不正确的是( )
| A、臭氧比氧气的氧化性更强,常温下能将银、汞等较不活泼的金属氧化 |
| B、臭氧是比氯水更好的消毒剂,因为它在消灭细菌后变成O2,无污染 |
| C、臭氧和活性炭一样,能够吸附有机色素,是种很好的漂白剂 |
| D、臭氧和氧气在一定条件下可以相互转化 |
 浓硫酸和2mol?L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )
浓硫酸和2mol?L-1的稀硫酸,在实验室中敞口放置.它们的质量和放置天数的关系如图,分析a、b曲线变化的原因是( )| A、a升华、b冷凝 |
| B、a挥发、b吸水 |
| C、a蒸发、b潮解 |
| D、a冷凝、b吸水 |
下列关于铵盐的叙述中正确的是( )
①所有铵盐中,氮元素化合价都是-3价;
②所有铵盐都溶于水;
③铵态氮肥不宜与草木灰混合使用;
④铵盐都是离子化合物;
⑤铵盐都能与碱反应,不能与酸反应.
①所有铵盐中,氮元素化合价都是-3价;
②所有铵盐都溶于水;
③铵态氮肥不宜与草木灰混合使用;
④铵盐都是离子化合物;
⑤铵盐都能与碱反应,不能与酸反应.
| A、①③④ | B、②③④ |
| C、①②③④ | D、①②③④⑤ |
对于溶液间进行的反应,对反应速率影响最小的因素是( )
| A、温度 | B、浓度 | C、压强 | D、催化剂 |
能说明某烃分子里含有碳碳不饱和键的叙述中正确的是( )
| A、分子组成中含碳氢原子数比为1:2 |
| B、完成燃烧生产等物质的量的CO2和H2O |
| C、能与溴加成反应而使溴水褪色,还能使KMnO4酸性溶液褪色 |
| D、空气中燃烧能产生黑烟 |
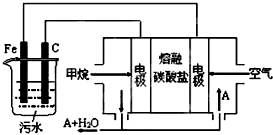 工业上采用的一种污水处理方法是:保持污水的pH在5.0-6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.某科研小组用此法处理污水,设计装置示意图,如图所示.
工业上采用的一种污水处理方法是:保持污水的pH在5.0-6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.某科研小组用此法处理污水,设计装置示意图,如图所示.