题目内容
9.元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个未成对电子,B的3p轨道上有空轨道,A、B同主族,B、C同周期,C是本周期中电负性最大的.请回答:
(1)A原子的核外电子排布图
 B原子的核外电子排布式1s22s22p63s23p2,C原子的价电子排布式3s23p5.C原子结构示意图
B原子的核外电子排布式1s22s22p63s23p2,C原子的价电子排布式3s23p5.C原子结构示意图
(2)A、B、C的气态氢化物中最不稳定的是SiH4.(填化学式)
(3)它们的最高价氧化物的水化物中,酸性最强的是HClO4.(填化学式)
(4)AC4的化学式CCl4,电子式
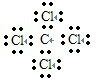 ,结构式
,结构式 ,中心原子Asp3杂化,立体构型是非极性 (填“极性”或“非极性”)分子.
,中心原子Asp3杂化,立体构型是非极性 (填“极性”或“非极性”)分子.
分析 元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个电子,则A的外围电子排布为2s22p2,故A为碳元素;B的3p轨道上有空轨道,则B的外围电子排布为3s23p1或3s23p2,A、B同主族,故B为硅元素;B、C同周期,C是本周期中电负性最大的,故C为氯元素,以此解答该题.
解答 解:元素A、B、C都是短周期元素,A元素原子的2p轨道上只有两个电子,则A的外围电子排布为2s22p2,故A为碳元素;B的3p轨道上有空轨道,则B的A的外围电子排布为3s23p1或3s23p2,A、B同主族,故B为硅元素;B、C同周期,C是本周期中电负性最大的,故C为氯元素.
(1)A为碳元素,碳原子的 ;B为硅元素,Si原子的核外电子排布式为1s22s22p63s23p2;C为氯元素C原子的核外电子排布式为1s22s22p63s23p5,价电子排布式为3s23p5,氯原子是17号元素,核外电子分为三个电子层,一层2个电子,二层8个电子.三层7个电子,原子结构示意图为
;B为硅元素,Si原子的核外电子排布式为1s22s22p63s23p2;C为氯元素C原子的核外电子排布式为1s22s22p63s23p5,价电子排布式为3s23p5,氯原子是17号元素,核外电子分为三个电子层,一层2个电子,二层8个电子.三层7个电子,原子结构示意图为 ,
,
故答案为: ;1s22s22p63s23p2;3s23p5;
;1s22s22p63s23p2;3s23p5; ;
;
(2)A为碳元素,B为硅元素,C为氯元素,它们气态氢化物的化学式分别是CH4、SiH4、HCl,非金属性越强,氢化物越稳定,非金属性Cl>C>Si,所以氢化物稳定性HCl>CH4>SiH4,气态氢化物最不稳定的化学式是SiH4,
故答案为:SiH4;
(3)非金属性越强,最高价氧化物的水化物酸性越强,非金属性Cl>C>Si,所以酸性HClO4>H2CO3>H2SiO3,酸性最强的是 HClO4,故答案为:HClO4;
(4)AC4的化学式CCl4,分子中碳原子与氯原子之间形成1对共用电子对,电子式为 ,结构式为
,结构式为 ,中心原子C原子的杂化轨道数为4,碳原子采取sp3杂化,分子为正四面体对称结构,是非极性分子,
,中心原子C原子的杂化轨道数为4,碳原子采取sp3杂化,分子为正四面体对称结构,是非极性分子,
故答案为:CCl4; ;
; ;sp3;非极性.
;sp3;非极性.
点评 本题考查结构与物质关系,为高考常见题型,侧重于学生的分析能力的考查,题目侧重考查核外电子排布规律、常用化学用语、分子结构等,难度不大,注意基础知识的掌握与理解.

| A. | ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | 第三周期元素的离子半径从左到右逐渐减小 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | ⅣA族元素的氢化物中,稳定性最好的是CH4 |
| A. | 油脂 | B. | 葡萄糖 | C. | 蛋白质 | D. | 淀粉 |
| A. | 锌片溶解了32.5 g | B. | 锌片增重32.5 g | ||
| C. | 铜片上析出lgH2 | D. | 铜片上析出1molH2 |
| A. | CH3CH2Cl | B. | CH3CH2CBr(CH3)2 | C. | CH3CH2CH2OH | D. | CH3OH |
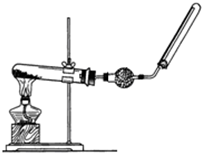 实验室中若用如图所示的装置制取并收集干燥的氨气.
实验室中若用如图所示的装置制取并收集干燥的氨气.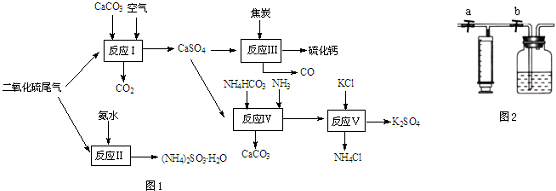
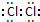 ;
;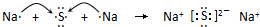 .
. 的系统命名:3,4-二甲基己烷
的系统命名:3,4-二甲基己烷 的键线式:
的键线式:
