题目内容
下列相关离子方程式书写正确的是( )
| A、NaClO溶液与FeCl2溶液混合:6Fe2++3ClO-+3H2O═2Fe(OH)3↓+3Cl-+4Fe3+ | ||||
| B、用食醋检验牙膏中的碳酸钙:CaCO3+2H+═Ca2++CO2↑+H2O | ||||
| C、FeCl2酸性溶液放在空气中变质:2Fe2++4H++O2═2Fe3++2H2O | ||||
D、电解MgCl2水溶液的离子方程式:2Cl-+2H2O
|
考点:离子方程式的书写
专题:
分析:A.二价铁离子具有强的还原性能够被次氯酸根离子氧化;
B.醋酸为弱电解质应保留化学式;
C.电荷不守恒;
D.氢氧化镁为沉淀应保留化学式.
B.醋酸为弱电解质应保留化学式;
C.电荷不守恒;
D.氢氧化镁为沉淀应保留化学式.
解答:
解:A.NaClO溶液与FeCl2溶液混合,离子方程式:6Fe2++3ClO-+3H2O═2Fe(OH)3↓+3Cl-+4Fe3+,故A正确;
B.用食醋检验牙膏中的碳酸钙,离子方程式:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故B错误;
C.FeCl2酸性溶液放在空气中变质,离子方程式为:4Fe2++4H++O2=4Fe3++2H2O,故C错误;
D.电解MgCl2水溶液的离子方程式,离子方程式为:2Cl-+Mg2++2H2O
H2↑+Cl2↑+2Mg(OH)2↓,故D错误;
故选:A.
B.用食醋检验牙膏中的碳酸钙,离子方程式:CaCO3+2CH3COOH═Ca2++CO2↑+H2O+2CH3COO-,故B错误;
C.FeCl2酸性溶液放在空气中变质,离子方程式为:4Fe2++4H++O2=4Fe3++2H2O,故C错误;
D.电解MgCl2水溶液的离子方程式,离子方程式为:2Cl-+Mg2++2H2O
| ||
故选:A.
点评:本题考查了离子方程式的书写,为高考频考点,明确反应的实质是解题关键,书写时应注意化学式的拆分、遵循原子个数电荷数守恒规律,选项D为易错选项.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案
相关题目
碘是一种与人的生命活动密切相关的元素,已知I2能溶于NaOH或KI溶液,反应方程式分别为:3I2+6OH-═5I-+IO
+3H2O(HIO不稳定,易发生歧化反应)和I2+I-═I
,溴化碘(IBr)是一种卤素互化物,具有与卤素单质相似的性质,下列反应方程式中不正确的是( )
- 3 |
- 3 |
| A、IBr加入Na2S溶液中产生黄色浑浊:IBr+S2-═I-+Br-+S↓ | ||
B、IBr加入KI溶液中:IBr+2I-═Br-+I
| ||
| C、IBr加入NaOH溶液中:IBr+2OH-═BrO-+I-+H2O | ||
D、IBr加入AgNO3溶液中:3IBr+5Ag++3H2O═3AgBr↓+2AgI↓+IO
|
设阿伏加德罗常数为NA,请你判断下列叙述中正确的是( )
| A、2NA个HF分子所占的体积约为44.8L |
| B、46 g四氧化二氮和二氧化氮的混合气体中含有的原子数少于3NA |
| C、常温常压下,8.8 gCO2和N2O混合气体中所含的电子数为4.4NA |
| D、5.6 g铁与500 mL 2 mol?L-1硝酸反应,转移的电子数为0.2NA |
下列对摩尔(mol)的有关说法中错误的是( )
| A、摩尔是一个单位而非物理量 |
| B、摩尔既能用来计量纯净物,又能用来计量混合物 |
| C、1mol任何气体所含气体的分子数目都相等 |
| D、H2的摩尔质量是2g |
下列离子方程式正确的是( )
A、等物质的量浓度的FeBr2和CuCl2混合溶液用惰性电极电解最初发生反应:Cu2++2Br-
| ||||
| B、碳酸氢镁溶液中加入足量的烧碱溶液:Mg2++2HCO3-+2OH-═MgCO3↓+CO32-+2H2O | ||||
| C、过量SO2通入氨水中:SO2+2NH3?H2O═2NH4++SO32-+H2O | ||||
| D、碳酸钙溶于醋酸:CaCO3+2H+═Ca2++CO2↑+H2O |
下列有关化学用语表示正确的是( )
| A、葡萄糖的结构简式:C6H12O6 | ||
| B、NaHCO3的电离:NaHCO3═Na++H++CO32- | ||
C、质子数为53、中子数为78的碘原子:
| ||
D、CO2的电子式: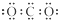 |
下列有关物质分类正确的是( )
| A、液氯、冰水混合均为纯净物 |
| B、NO2、CO、CO2均为酸性氧化物 |
C、 与 与 互为同系物 互为同系物 |
| D、淀粉、纤维素和油脂都属于天然高分子化合物 |
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ?mlo-1-1411.0kJ?mlo-1和-1366.8kJ?mlo-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( )
| A、-44.2kJ?mol-1 |
| B、+44.2kJ?mol-1 |
| C、-330kJ?mol-1 |
| D、+330kJ?mol-1 |
在m A(g)+n B(g)?p C(g)+q D(g)的反应中,(m、n、p、q为各物质的化学计量数),经5min达到平衡,测得:A增加3mol?L-1,B增加1mol?L-1,C减少2mol?L-1,此时若给体系加压,平衡不移动,则m:n:p:q为( )
| A、2:3:2:3 |
| B、2:2:3:3 |
| C、3:1:2:2 |
| D、3:1:2:3 |