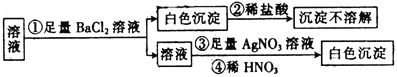
题目内容
【题目】现有A、B两种烃,已知A的分子式为C5Hm,而B的最简式为C5Hn(m、n均为正整数)。
(1)下列关于烃A和烃B的说法中不正确的是_____(填字母编号)。
a、烃A和烃B可能互为同系物
b、烃A和烃B可能互为同分异构体
c、当m=12时,烃A一定为烷烃
d、当n=11时,烃B可能的分子式有两种
e、烃A和烃B可能都为芳香烃
(2)若烃A为链状烃,且分子中所有碳原子都在一条直线上,则A的结构简式为____。
(3)若烃A为链状烃,分子中所有碳原子不可能都在同一平面上。在一定条件下,1mol A最多只能与1mol H2发生加成反应。写出烃A的名称:_______。
(4)若烃B为苯的同系物,取一定量的烃B完全燃烧后,生成物先通过足量浓硫酸,浓硫酸增重1.26g,再通过足量碱石灰,碱石灰增重4.4g,则烃B的分子式为______。
(5)有机物CH3CH(C2H5)CH(CH3)(CH2)3 CH3的系统命名是_______,1mol该有机物完全燃烧需消耗标准状况下氧气___L。
(6)请写出下列化合物所含官能团的名称:
①CH3CH=CH2:______; ② :______; ③
:______; ③ :______。
:______。
【答案】de ![]() 3-甲基-1-丁烯 C10H14 3,4-二甲基辛烷 347.2 碳碳双键 羟基 酯基
3-甲基-1-丁烯 C10H14 3,4-二甲基辛烷 347.2 碳碳双键 羟基 酯基
【解析】
(1)a、当A为C5H10,B为C10H20的烯烃时,烃A和烃B互为同系物, a项正确;
b、当m=n时,A与B分子式相同,结构不同时,互为同分异构体;
c、烷烃的通式是CnH2n+2(n≥1);
d、当n=11时,最简式为C5H11的有机物只能是C10H22;
e、烃A的分子中只含有5个碳原子,不能形成芳香烃;
(2)与碳碳三键直接相连的原子共线,因此,要使5个碳原子共线,结构中需含有2个碳碳三键;
(3)链烃A与H2最多以1:1加成,可知A为烯烃C5H10,分子中所有碳原子不可能共面,说明碳原子形成了四面体结构;
(4)B完全燃烧后,生成物先通过足量浓硫酸,浓硫酸增重1.26g,增重的质量为水的质量,再通过足量碱石灰,碱石灰增重4.4g,增重的是CO2的质量,计算C和H的物质的量求比值可得分子式;
(5)根据有机物的结构简式找到最长的碳链,编号确定支链的位置进行命名,根据分子式确定完全燃烧消耗氧气的体积;
(6)根据有机物的结构确定官能团的名称。
(1)a、当A为C5H10,B为C10H20的烯烃时,烃A和烃B互为同系物;
b、当m=n时,A与B分子式相同,结构不同时,互为同分异构体,b项正确;
c、烷烃的通式是CnH2n+2(n≥1),当m=12时,分子式为C5H12,符合烷烃的通式,属于烷烃,c项正确;
d、当n=11时,最简式为C5H11的有机物只能是C10H22,d项错误;
e、烃A的分子中只含有5个碳原子,不可能形成芳香烃,e项错误;
因此错误的是de;
(2)与碳碳三键直接相连的原子共线,因此,要使5个碳原子共线,结构中需含有2个碳碳三键,因此有机物A为:![]() ;
;
(3)链烃A与H2最多以1:1加成,可知A为烯烃C5H10,分子中所有碳原子不可能共面,说明碳原子形成了四面体结构,该有机物为3-甲基-1-丁烯;
(4)n(CO2)=![]() =0.1mol,n(H2O)=
=0.1mol,n(H2O)=![]() =0.07mol,n(H)=0.07mol×2=0.14mol,n(C):n(H)=0.1:0.14=5:7,因此最简式为C5H7,B为苯的同系物,通式为CnH2n-6,n:(2n-6)=5:7,解得n=10,所以B的分子式为C10H14;
=0.07mol,n(H)=0.07mol×2=0.14mol,n(C):n(H)=0.1:0.14=5:7,因此最简式为C5H7,B为苯的同系物,通式为CnH2n-6,n:(2n-6)=5:7,解得n=10,所以B的分子式为C10H14;
(5)根据有机物的结构简式可知,最长的碳链上有8个碳原子,为辛烷,在3号碳和4号碳上分别连有一个甲基,因此该有机物的名称为3,4-二甲基辛烷;该有机物的分子式为C10H22,1mol该有机物完全燃烧时消耗氧气的物质的量为10+![]() =15.5mol,标况下的体积为:15.5mol×22.4L/mol=347.2L;
=15.5mol,标况下的体积为:15.5mol×22.4L/mol=347.2L;
(6)根据有机物的结构可知:①中的官能团为碳碳双键;②中的官能团为羟基;③中的官能团为酯基。

 全能练考卷系列答案
全能练考卷系列答案【题目】某化学小组采用类似制乙酸乙酯的装置用环己醇制备环己烯,装置如图1所示。

已知: +H2O。
+H2O。
密度/ g·cm-3 | 熔点/℃ | 沸点/℃ | 溶解性 | |
环己醇 | 0.96 | 25 | 161 | 能溶于水 |
环己烯 | 0.81 | -103 | 83 | 难溶于水 |
(1)制备粗品
将12.5mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品。
①试管A中碎瓷片的作用是___,导管B除了导气外还具有的作用是__。
②将试管C置于冰水中的目的是__。
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等。加入饱和食盐水,振荡、静置、分层,环己烯在___(填“上”或“下”)层,分液后用___(填字母)洗涤。
a.酸性KMnO4溶液 b.稀硫酸 c.Na2CO3溶液
②再将提纯后的环己烯按如图2所示装置进行蒸馏,冷却水从__(填字母)口进入,目的是___。蒸馏时要加入生石灰,目的是___。

③收集产品时,应控制温度在___左右,实验制得的环己烯精品质量低于理论产量,可能的原因是___(填字母)。
a.蒸馏时从70℃开始收集产品
b.环己醇实际用量多了
c.制备粗产品时环己醇随产品一起蒸出
(3)以下用来区分环己烯精品和粗品的试剂或方法中,合理的是__(填字母)。
a.酸性高锰酸钾溶液 b.金属钠 c.测定沸点
【题目】A、B、C、D、E五种元素均位于前四周期,原子序数逐渐增大,只有两种是金属元素。A、B、D三种元素在周期表中相对位置如图,其中A的价层电子排布为ns2np3,C的基态原子的第I电离能远小于第II电离能。E是第四期第IB族元素,回答下列问题:
A | B | |
D |
⑴E原子的基态电子排布式 ______;
⑵A、B、C三种元素的第I电离能由大到小的顺序是 ______;
⑶D能形成多种价态的含氧酸,其酸性由强到弱的顺序为 ______;
⑷已知金属C单质的晶胞为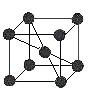 ,则C原子的堆积方式为 ______ ,C原子的配位数是 ______ ;
,则C原子的堆积方式为 ______ ,C原子的配位数是 ______ ;
⑸向E、D形成的稳定化合物溶液中不断加入A的常见氢化物水溶液,最后E的最主要存在形式为![]() 写真实符号
写真实符号![]() ______。
______。