题目内容
对下列实验现象的原因分析不 正确的一项是( )
| 选项 | 实验现象 | 原因分析 |
| A | 浓的硫化钠溶液有臭味 | 硫离子多步水解生成硫化氢,硫化氢有臭味 |
| B | 新制氯水中滴加石蕊试液,溶液先变红,后褪色 | 氯气与水反应生成HCl、HClO,HCl显强酸性,使石蕊变红,HClO具有强氧化性,使其褪色 |
| C | SO2通入溴水中,溴水褪色 | SO2具有漂白性,使其褪色 |
| D | 向湿润蔗糖中加入浓硫酸,固体迅速变黑,后体积急剧膨胀 | 在浓硫酸脱水作用下,蔗糖被炭化,炭与浓硫酸反应生成了CO2、SO2 |
| A、A | B、B | C、C | D、D |
考点:浓硫酸的性质,氯气的化学性质,二氧化硫的化学性质
专题:卤族元素,氧族元素
分析:A、硫离子水解会得到硫化氢,硫化氢是有臭鸡蛋气味的气体;
B、氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性;
C、二氧化硫具有还原性,能被溴单质氧化为硫酸;
D、浓硫酸具有脱水性,能和单质碳之间发生反应生成CO2和SO2.
B、氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性;
C、二氧化硫具有还原性,能被溴单质氧化为硫酸;
D、浓硫酸具有脱水性,能和单质碳之间发生反应生成CO2和SO2.
解答:
解:A、浓硫化钠溶液中硫离子水解会得到硫化氢,硫化氢是有臭鸡蛋气味的气体,所以浓硫化钠溶液有臭味,故A正确;
B、氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性,所以溶液先变红,后褪色,故B正确;
C、SO2通入溴水中,溴水褪色是因为:二氧化硫具有还原性,能和溴单质之间反应生成硫酸和氢溴酸,导致溶液褪色,故C错误;
D、浓硫酸具有脱水性,向湿润蔗糖中加入浓硫酸,固体迅速变黑,蔗糖被炭化,并且炭与浓硫酸反应生成了CO2和SO2,故D正确.
故选C.
B、氯气与水反应生成HCl、HClO,呈酸性,使石蕊变红,HClO具有强氧化性、漂白性,所以溶液先变红,后褪色,故B正确;
C、SO2通入溴水中,溴水褪色是因为:二氧化硫具有还原性,能和溴单质之间反应生成硫酸和氢溴酸,导致溶液褪色,故C错误;
D、浓硫酸具有脱水性,向湿润蔗糖中加入浓硫酸,固体迅速变黑,蔗糖被炭化,并且炭与浓硫酸反应生成了CO2和SO2,故D正确.
故选C.
点评:本题涉及浓硫酸和二氧化硫的性质,注意知识的归纳和整理是解题的关键,难度不大.

练习册系列答案
相关题目
己烯雌酚是一种激素类药物,结构如下.下列有关叙述中不正确的是( )
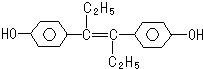

| A、该有机物分子中,至少8个碳原子一定共平面 |
| B、可与NaOH和NaHCO3发生反应 |
| C、1mol该有机物可以与5mol Br2发生反应 |
| D、它易溶于有机溶剂 |
已知1mol某态烃CmHn完全燃烧时,需要耗氧气5mol;则m与n的下列关系正确的是( )
| A、m=8+n | ||
| B、m=10-n | ||
C、m=5-
| ||
| D、m=12-n |
在恒温恒容条件下,将4molA和2molB放入一密闭容器中2A(g)+B(g)?2C(g)+D(s),达到平衡时,C的体积分数为a;在相同条件下,按下列配比分别投放A、B、C、D,达到平衡时,C的体积分数不等于a的是( )
| A、4mol、2mol、0mol、2mol |
| B、2mol、1mol、2mol、2mol |
| C、2mol、1mol、2mol、1mol |
| D、2mol、1mol、0mol、1mol |
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是( )
| A、含氧酸的酸性:X对应的酸性强于Y对应的酸性 |
| B、第一电离能Y不一定小于X |
| C、X与Y形成化合物时,X显负价,Y显正价 |
| D、Y的气态氢化物的稳定性小于X气态氢化物的稳定性 |
下列微粒中,只具有还原性的是( )
| A、Na+ |
| B、F2 |
| C、Cl- |
| D、SO32- |
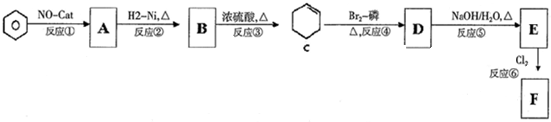
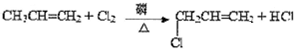 F的结构简式为
F的结构简式为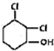
 直接制
直接制 ,理由是
,理由是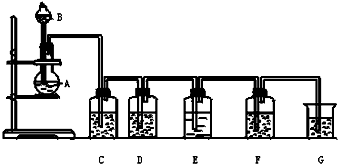 实验室用如图所示装置制备氯气(加热装置略去),并进行氯气性质实验,请回答下列问题:
实验室用如图所示装置制备氯气(加热装置略去),并进行氯气性质实验,请回答下列问题: