��Ŀ����
 A��B��D��X��Y���ɶ�����Ԫ����ɵĻ��������X�dz�����ǿ�ᣨ�����ᣩ��Y�dz�����ǿ����������ƣ������ǵ��ת����ϵ����ͼ�������������ˮ��ȥ����
A��B��D��X��Y���ɶ�����Ԫ����ɵĻ��������X�dz�����ǿ�ᣨ�����ᣩ��Y�dz�����ǿ����������ƣ������ǵ��ת����ϵ����ͼ�������������ˮ��ȥ������1����A��B��Ϊ���壬��ˮ��Һ�з�Ӧ����D������A����Ư���ԣ���B�ĵ���ʽΪ
��2����A��B��D������ͬ�Ľ���Ԫ�أ���ҵ�õ������������ķ�����ȡ�ý������ʣ��ֽ�Y����A����Һ�����������۲쵽��������
��3����A��һ���������壬����B��D��Yʱ�����Ϊ��ɫ��д��D+Y��B �����ӷ���ʽ
��4����D�ǵ�������������ˮ����������һ�֣���A��B���ܷ�Ӧ����D����D��������
���㣺������ƶ�
ר�⣺�ƶ���
��������1����A��B��Ϊ���壬��ˮ��Һ�з�Ӧ����D������A����Ư���ԣ���AΪSO2��D����ǿ�Ӧ�õ�����B��DΪ��Σ�����֪BΪNH3��DΪ��NH4��2SO3��������������������NO��ˮ��
��2����A��B��D������ͬ�Ľ���Ԫ�أ���AΪ���Ρ�BΪƫ�����Ρ�DΪAl��OH��3��
��3������B��D��Yʱ�����Ϊ��ɫ��������NaԪ�أ�A��һ���������壬��AΪCO2��BΪNa2CO3��DΪNaHCO3��YΪNaOH��
��4����D�ǵ�������������ˮ����������һ�֣���A��B���ܷ�Ӧ����D����DΪH2N-CH2-COOH��
��2����A��B��D������ͬ�Ľ���Ԫ�أ���AΪ���Ρ�BΪƫ�����Ρ�DΪAl��OH��3��
��3������B��D��Yʱ�����Ϊ��ɫ��������NaԪ�أ�A��һ���������壬��AΪCO2��BΪNa2CO3��DΪNaHCO3��YΪNaOH��
��4����D�ǵ�������������ˮ����������һ�֣���A��B���ܷ�Ӧ����D����DΪH2N-CH2-COOH��
���
�⣺��1����A��B��Ϊ���壬��ˮ��Һ�з�Ӧ����D������A����Ư���ԣ���AΪSO2��D����ǿ�Ӧ�õ�����B��DΪ��Σ�����֪BΪNH3��DΪ��NH4��2SO3���������ӵ���ʽΪ ��������������������NO��ˮ����Ӧ����ʽΪ��4NH3+5O2
��������������������NO��ˮ����Ӧ����ʽΪ��4NH3+5O2
4NO+6H2O��
�ʴ�Ϊ�� ��4NH3+5O2
��4NH3+5O2
4NO+6H2O��
��2����A��B��D������ͬ�Ľ���Ԫ�أ���AΪ���Ρ�BΪƫ�����Ρ�DΪAl��OH��3����ǿ��B����������Һ�У�����������������ɫ�������������������ܽ⣬
�ʴ�Ϊ�������ɰ�ɫ����������ʧ��
��3������B��D��Yʱ�����Ϊ��ɫ��������NaԪ�أ�A��һ���������壬��AΪCO2��BΪNa2CO3��DΪNaHCO3��YΪNaOH����
D+Y��B �����ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O��
��״����11.2L������̼�����ʵ���=
=0.5mol��600mL 1mol/L ��Na2CO3��Һ��Na2CO3�����ʵ���=0.6L��1mol/L=0.6mol�����߷�����Ӧ��CO2+Na2CO3+H2O=2NaHCO3���ʶ�����̼��ȫ��Ӧ���õ�1molNaHCO3������0.5molNa2CO3��ʣ��Na2CO3�����ʵ���=0.6mol-0.5mol=0.1mol������Һ��n��Na2CO3����n��NaHCO3��=0.1mol��1mol=1��10��
�ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��n��Na2CO3����n��NaHCO3��=1��10��
��4����D�ǵ�������������ˮ����������һ�֣���A��B���ܷ�Ӧ����D����DΪH2N-CH2-COOH������Ϊ�ʰ��ᣬ��NaOH��Ӧ�Ļ�ѧ����ʽΪ��H2N-CH2-COOH+NaOH��H2N-CH2-COONa+H2O�������ᷴӦ�Ļ�ѧ����ʽΪ��H2N-CH2-COOH+HCl��HOOC-CH2-NH3+Cl-��
�ʴ�Ϊ���ʰ��H2N-CH2-COOH+NaOH��H2N-CH2-COONa+H2O��H2N-CH2-COOH+HCl��HOOC-CH2-NH3+Cl-��
 ��������������������NO��ˮ����Ӧ����ʽΪ��4NH3+5O2
��������������������NO��ˮ����Ӧ����ʽΪ��4NH3+5O2
| ||
| �� |
�ʴ�Ϊ��
 ��4NH3+5O2
��4NH3+5O2
| ||
| �� |
��2����A��B��D������ͬ�Ľ���Ԫ�أ���AΪ���Ρ�BΪƫ�����Ρ�DΪAl��OH��3����ǿ��B����������Һ�У�����������������ɫ�������������������ܽ⣬
�ʴ�Ϊ�������ɰ�ɫ����������ʧ��
��3������B��D��Yʱ�����Ϊ��ɫ��������NaԪ�أ�A��һ���������壬��AΪCO2��BΪNa2CO3��DΪNaHCO3��YΪNaOH����
D+Y��B �����ӷ���ʽΪ��HCO3-+OH-=CO32-+H2O��
��״����11.2L������̼�����ʵ���=
| 11.2L |
| 22.4L/mol |
�ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��n��Na2CO3����n��NaHCO3��=1��10��
��4����D�ǵ�������������ˮ����������һ�֣���A��B���ܷ�Ӧ����D����DΪH2N-CH2-COOH������Ϊ�ʰ��ᣬ��NaOH��Ӧ�Ļ�ѧ����ʽΪ��H2N-CH2-COOH+NaOH��H2N-CH2-COONa+H2O�������ᷴӦ�Ļ�ѧ����ʽΪ��H2N-CH2-COOH+HCl��HOOC-CH2-NH3+Cl-��
�ʴ�Ϊ���ʰ��H2N-CH2-COOH+NaOH��H2N-CH2-COONa+H2O��H2N-CH2-COOH+HCl��HOOC-CH2-NH3+Cl-��
���������⿼�������ƶϣ���Ҫѧ����������Ԫ�ػ�����֪ʶ��ע�⣨4���а��������ᡢ��ķ�Ӧ���Ѷ��еȣ�

��ϰ��ϵ�д�
 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
�����Ŀ
������������Һ�п��Դ��������һ���ǣ�������
| A��K+��Na+��SO42- |
| B��K+��H+��OH- |
| C��Na+��Ag+��Cl- |
| D��Ca2+��OH-��CO32- |
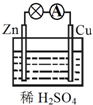 ������ͼ��ʾ��ԭ��أ�����˵������ȷ���ǣ�������
������ͼ��ʾ��ԭ��أ�����˵������ȷ���ǣ�������| A��CuΪ������ZnΪ���� |
| B����װ���ܽ���ѧ��ת��Ϊ���� |
| C��������ͭƬͨ����������пƬ |
| D��������ӦΪ 2H++2e-�TH2�� |
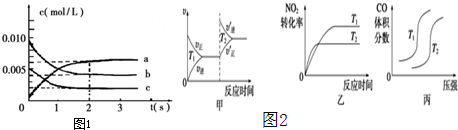 ���Ǵ����к����������壬�о������仯�������������Ҫ�����壮
���Ǵ����к����������壬�о������仯�������������Ҫ�����壮 ��һ�������½��л�ѧ��Ӧ����������µ�ת����ϵ�ش��������⣬
��һ�������½��л�ѧ��Ӧ����������µ�ת����ϵ�ش��������⣬