题目内容
17.根据元素周期表推测Fe元素在周期表中位于第四周期( )| A. | 第ⅢB族 | B. | 第Ⅲ族 | C. | 第VⅢ族 | D. | 第VⅢB族 |
分析 铁的原子序数为26,位于周期表第四周期,第8列,以此解答该题.
解答 解:铁的原子序数为26,位于周期表第四周期,第8列,而8、9、10三列为第VⅢ族.
故选C.
点评 本题考查元素周期表及应用,把握元素在周期表的位置、周期表的结构为解答的关键,注重基础知识的考查,题目难度不大.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案
相关题目
14.用NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 78g Na2O2中含有的离子总数为4NA | |
| B. | 标准状况下,1.12L HF中所含的分子总数为0.05NA | |
| C. | 由CO2和O2组成的混合物共有NA个分子,其中的氧原子数为2NA | |
| D. | 0.11mol•L-1 FeCl3溶液中含有的Cl-数目为0.3NA |
15.下列元素的原子半径最大的是( )
| A. | Na | B. | Al | C. | S | D. | Cl |
5. KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
 KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )
KClO3和 KHSO3可发生下列反应:ClO3-+HSO3-→SO42-+Cl-+H+(未配平),已知酸性越强,该反应的反应速率越快.如图为反应速率v(ClO3-)随时间(t)的变化曲线.下列有关说法不正确的( )| A. | KClO3和 KHSO3发生反应的氧化剂与还原剂的物质的量之 比为1:3 | |
| B. | 反应开始阶段速率逐渐增大可能是 c(H+)逐渐增高导致的 | |
| C. | 反应后期速率逐渐减小的主要原因是 c(ClO3 )、c(HSO3)降低 | |
| D. | 纵坐标为 v(HSO3-)时 v-t 的曲线与原图曲线完全吻合 |
12.对人体健康不会造成危害的事实是( )
| A. | 用工业酒精(含甲醇)兑制饮用白酒 | |
| B. | 用福尔马林浸泡海产品进行防腐保鲜 | |
| C. | 长期饮用长时间反复加热沸腾的水 | |
| D. | 在食用盐中加入碘酸钾以消除碘缺乏病 |
2.下列实验装置不能达到实验目的是( )
| A. | 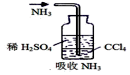 用稀硫酸吸收氨气 | B. | 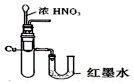 验证Cu与浓硝酸反应的热量变化 | ||
| C. |  萃取时振荡分液漏斗 | D. | 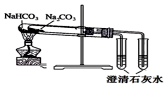 比较Na2CO3与NaHCO3的热稳定性 |
9.下列说法正确的是( )
| A. | 在元素周期表中,s区、d区和ds区的元素都是金属 | |
| B. | 在元素周期表中,每个纵列的价电子层的电子总数一定相等 | |
| C. | 某基态原子错误的核外电子排布图为 ,该排布图违背了泡利原理 ,该排布图违背了泡利原理 | |
| D. | 在氢原子的基态电子的概率分布图中,小黑点的疏密程度表示电子在该区域空间出现概 率的大小 |
6.下列关于苯的说法中,正确的是( )
| A. | 苯分子为平面正六边形结构,6个碳原子之间的键完全相同 | |
| B. | 从苯的结构看,分子中含有单、双键,所以能使酸性高锰酸钾溶液和溴的四氯化碳溶液因反应而褪色 | |
| C. | 在催化剂存在下,苯能与溴水发生取代反应,生成溴苯 | |
| D. | 苯是一种密度比水大,不溶于水的有特殊气味的无色液体 |
5.为了达到下表所列的实验目的,请选择合适的实验方法,将其标号填入对应的空格中.
实验方法:
A.加入足量铁粉,过滤
B.加热
C.加入硝酸银溶液
D.滴入酚酞试液.
| 实验目的 | 实验方法 |
| 除去Na2CO3固体中少量的NaHCO3 | |
| 检验自来水中是否含有Cl- | |
| 证明NaOH溶液呈碱性 | |
| 除去FeCl2溶液中少量的FeCl3 |
A.加入足量铁粉,过滤
B.加热
C.加入硝酸银溶液
D.滴入酚酞试液.