题目内容
3.某有机物其结构简式为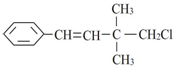 ,关于该有机物,下列叙述不正确的是( )
,关于该有机物,下列叙述不正确的是( )| A. | 所有碳原子不可能在同一平面上 | |
| B. | 属于卤代烃 | |
| C. | 分子式为C12H15Cl | |
| D. | 能发生加成反应、取代反应、加聚反应、消去反应 |
分析 有机物含有碳碳双键和氯原子,结合烯烃、氯代烃的性质以及有机物的结构特点解答该题.
解答 解:A.分子中含有饱和碳原子,具有甲烷的结构特点,则所有碳原子不可能在同一平面上,故A正确;
B.含有氯原子,属于卤代烃,故B正确;
C.根据结构简式可知有机物分子式为C12H15Cl,故C正确;
D.氯原子邻位碳原子没有氢原子,不能发生消去反应,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高考常见题型,注意把握官能团与性质的关系为解答的关键,熟悉烯烃、卤代烃的性质即可解答,题目难度不大.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案 小学学习好帮手系列答案
小学学习好帮手系列答案
相关题目
14.下列取代基或微粒中,碳原子都满足最外层为8电子结构的是( )
| A. | 苯 | B. | 乙基(-CH2CH3) | C. | 碳正离子[(CH3)3C+] | D. | 碳烯(:CH2) |
11. A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
请回答下列问题:
(1)Z的化学式为NO2.乙的结构式为N≡N.
(2)B的最高价氧化物的电子式为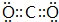 .
.
(3)用电子式表示A元素和E元素形成化合物的过程: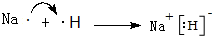 .
.
(4)G的单质与水反应的离子方程式Cl2+H2O?H++Cl-+HClO.
(5)F的单质与E的最高价氧化物的水化物反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(6)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.W空气燃料电池放电时负极反应式为N2H4+4OH--4e-=N2↑+4H2O.
 A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.
A、B、C、D、E、F、G是核电荷数依次增大的短周期主族元素,A元素原子的核外电子数、电子层数和最外层电子数均相等,元素B的一种常见单质可做惰性电极材料,C、D、G三种元素在周期表中的相对位置如图①所示,C、D、F的质子数之和等于E、G的质子数之和.E、F为金属元素,只有G元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、C、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、C两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质.它们之间的转化关系如图②所示.| C | D | |
| G |
(1)Z的化学式为NO2.乙的结构式为N≡N.
(2)B的最高价氧化物的电子式为
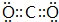 .
.(3)用电子式表示A元素和E元素形成化合物的过程:
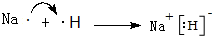 .
.(4)G的单质与水反应的离子方程式Cl2+H2O?H++Cl-+HClO.
(5)F的单质与E的最高价氧化物的水化物反应的离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑.
(6)W空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.W空气燃料电池放电时负极反应式为N2H4+4OH--4e-=N2↑+4H2O.
15.下列关于元素电负性大小的比较中,不正确的是( )
| A. | O<S<Se<Te | B. | C<N<O<F | C. | P<S<O<F | D. | K<Na<Mg<Al |



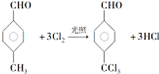 ,反应类型为取代反应
,反应类型为取代反应 +n
+n $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ +(2n-1)H2O
+(2n-1)H2O 的路线流程图:
的路线流程图: 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}CH_{2}OH}$CH3COOCH2CH3.