题目内容
3. 一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )| A. | 反应进行到5 s时,v(A)=v(B)=v(C)=v(D) | |
| B. | 反应进行到5 s时,B的平均反应速率为0.06mol/(L•s) | |
| C. | 反应进行到1 s时,v(A)=v(B) | |
| D. | 该反应的化学方程式为6A+2D?3B+4C |
分析 A.平衡状态时v(A):v(B):v(C):v(D)=系数之比;
B.反应进行到5 s时,B的平均反应速率根据v=$\frac{\frac{△n}{V}}{△t}$来计算;
C.反应进行到1 s时,A、B的物质的量变化量不等,根据v=$\frac{\frac{△n}{V}}{△t}$分析;
D.根据图象中的有关数据判断四种物质的变化,再根据计量数之比等于物质的量的变化量之比.
解答 解:A.反应进行到5 s时达到了平衡状态,根据v=$\frac{\frac{△n}{V}}{△t}$可知,各物质的反应速率与物质的量变化成正比,则v(A):v(B):v(C):v(D)=(1.2-0.2)mol:(1.0-0.4)mol:(1.0-0.2)mol:(0.4-0)mol=5:3:4:2,故A错误;
B.反应进行到5 s时,B的平均反应速率v=$\frac{\frac{1.0mol-0.4mol}{2L}}{5s}$=0.06mol/(L•s),故B正确;
C.反应进行到1 s时,n(A)=n(B),但是A、B的物质的量变化量不等,所以v(A)≠v(B),故C错误;
D.由图可知,反应达到平衡时A物质增加了1.0mol、D物质增加了0.4mol、B物质减少了0.6mol、C物质减小了0.8mol,所以A、D为生成物,B、C为反应物,且v(A):v(B):v(C):v(D)=(1.2-0.2)mol:(1.0-0.4)mol:(1.0-0.2)mol:(0.4-0)mol=5:3:4:2,所以该反应方程式为:3B+4C?5A+2D,故D错误;
故选B.
点评 本题考查了物质的量随反应时间的变化,题目难度中等,涉及反应速率计算、可逆反应方程式书写等知识,明确化学反应速率与化学计量数的关系为解答关键,试题培养了学生的灵活应用能力.

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案| A. | 1mol硫酸与足量氢氧化钠发生中和反应生成水所释放的热量称为中和热 | |
| B. | 化学能与其他形式的能相互转化的途径是化学反应 | |
| C. | 乙醇分子与水分子之间不仅存在范德华力还存在氢键 | |
| D. | 微粒半径K+<Cl?<S2? |


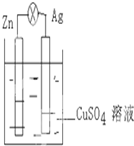 如图,在银锌原电池中,以硫酸铜溶液为电解质溶液.
如图,在银锌原电池中,以硫酸铜溶液为电解质溶液. 实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空:
实验室制取少量溴乙烷的装置如图所示.根据题意完成下列填空: