题目内容
11.在复杂体系中,确认化学反应先后顺序有利于解决问题.下列反应先后顺序判断正确的是( )| A. | 在含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入Zn:Ag+、Cu2+、H+、Fe2+ | |
| B. | 在含等物质的量的AlO2-、OH-、CO32-溶液中,逐滴加入盐酸:AlO2-、Al(OH)3、OH-、CO32- | |
| C. | 在含等物质的量的Ba(OH)2、KOH的溶液中通入CO2:KOH、Ba(OH)2、BaCO3 | |
| D. | 在含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2:I-、Br-、Fe2+ |
分析 A.氧化性强的先与Zn反应;
B.先发生OH-与酸的中和反应;
C.先发生钡离子与CO2反应再发生OH-与CO2反应;
D.先氧化碘离子,再氧化亚铁离子,最后氧化溴离子.
解答 解:A.氧化性由大到小的顺序为Ag+、Cu2+、H+、Fe2+,含等物质的量的Fe2+、Ag+、Cu2+、H+的溶液中加入Zn:Ag+、Cu2+、H+、Fe2+,故A正确;
B.含等物质的量的AlO2-、OH-、CO32-的溶液中,逐滴加入盐酸,反应的先后OH-、AlO2-、CO32-、Al(OH)3,故B错误;
C.含等物质的量的Ba(OH)2、KOH的溶液中通入CO2,先后顺序为Ba(OH)2、KOH、BaCO3,故C错误;
D.含等物质的量的FeBr2、FeI2的溶液中缓慢通入Cl2,反应的先后为I-、Fe2+、Br-,故D错误;
故选A.
点评 本题考查离子反应的先后顺序,为高频考点,侧重氧化的先后顺序及中和的先后顺序的考查,明确发生的反应先后顺序为解答的关键,题目难度中等.

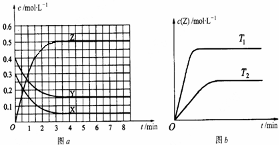
| A. | 该反应的正反应是放热反应 | |
| B. | T0时,该反应的平衡常数为$\frac{1}{3}$ | |
| C. | 反应时各物质的反应速率关系为:2v (X)=2v (Y)=v (Z) | |
| D. | 图a中反应达到平衡时,Y的转化率为37.5% |
| A. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液变红 | |
| B. | Na2O与Na2O2组成元素相同、阴阳离子个数比相同,但跟水反应的产物不同 | |
| C. | 只存在共价键的物质一定是共价化台物、离子化合物中一定含有离子键 | |
| D. | 元素原子的最外层电子数越多,得电子能力越强,失电子能力越弱 |
| A. |  甘油 甘油 | B. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | ||
| C. | 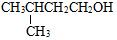 3-甲基-1-丁醇 3-甲基-1-丁醇 | D. | 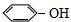 石碳酸 石碳酸 |

| A. | 溴水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 溴的CCl4溶液 | D. | 银氨溶液 |
下表是25℃时某些盐的浓度积常数和弱酸的电离平衡常数,下列说法正确的是( )
化学式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
Ksp或Ka | Ksp=1.8×10-10 | Ksp=2.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
A.相同浓度CH3COONa和NaClO的混合液中,各离子浓度的大小关系是
c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+)
B.碳酸钠溶液中滴加少量氯水的离子方程式H2O+2CO32-+Cl2=2HCO3-+Cl-+ClO-
C.向0.1mol/LCH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=9:5,此时溶液pH=5
D.向浓度均为1×10-3mol/L的KCl和K2CrO4混合液中滴加1×10-3mol/L的AgNO3溶液,CrO42-先形成沉淀
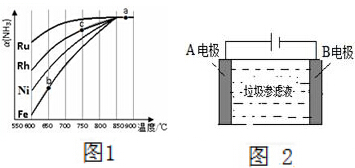 氨气在生产、生活和科研中应用十分广泛.
氨气在生产、生活和科研中应用十分广泛.