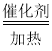题目内容
【题目】Ⅰ、下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______(填序号,下同);
(2)互为同素异形体的是_____;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___种;
Ⅱ、用化学用语回答下列问题:
(1)写出NaOH的电子式____;
(2)用电子式表示二氧化碳分子的形成过程_________;
Ⅲ、下列物质:①N2 ②H2O2 ③NH3 ④Na2O ⑤NH4Cl
(1)含有极性键和非极性键的是_______(填序号,下同);
(2)含有极性键的离子化合物是_________;
(3)氟化氢水溶液中存在的氢键有________种;
(4)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____。
【答案】①④ ③ 5 ![]()
![]() ② ⑤ 4 N C--CN
② ⑤ 4 N C--CN
【解析】
I.(1)同位素是质子数相同,中子数不同的同种元素不同原子的互称,因此互为同位素的是①④;
答案为①④;
(2)同素异形体是同种元素构成的不同结构的单质,互为同素异形体的是③;
答案为③
(3)氯化氢分子式为HCl,氢的三种原子与氯的两种原子两两组合,利用质量数近似等于相对原子质量,得到氯化氢的相对分子质量分别是36、38、37、39、40,有5种;
答案为5;
II.(1)NaOH为离子化合物,是由Na+和OH-组成,含有化学键为离子键和极性共价键,即NaOH的电子式为![]() ;
;
答案为![]() ;
;
(2)CO2为共价化合物,其结构式为O=C=O,因此表示CO2分子形成过程为 ;
;
答案为 ;
;
Ⅲ.①N2只含有非极性键,②H2O2的结构式为H-O-O-H,含有极性键和非极性键,③NH3只含有极性键,④Na2O属于离子化合物,只含有离子键,⑤NH4Cl是由NH4+和Cl-组成离子化合物,含有离子键和极性键,
(1)含有极性键和非极性键的是H2O2,即②;
答案为②;
(2)含有极性键的离子化合物是NH4Cl,即⑤;
答案为⑤;
(3)两个HF分子间形成氢键F-H…F,两个水分子间形成氢键O-H…F,HF与H2O分子间形成氢键F-H…O、O-H…F,HF的水溶液中存在的氢键形式有4种;
答案为4;
(4)C和N之间存在三键,且每个原子最外层均满足8电子稳定结构,即(CN)2的结构式为NC--CN;
答案为NC--CN。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】这次中美贸易战的矛盾激化,也让我们看到了中国半导体产业存在的诸多不足,俗话说“亡羊补牢,为时未晚”,找出存在的不足,然后针对地去解决问题,才能让半导体产业链发展壮大起来。三氯化氧磷(POCl3)是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料。一研究小组在实验室模拟反应![]() 制备POCl3并测定产品含量。
制备POCl3并测定产品含量。
资料卡片:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
PCl3 | -93.6 | 76.1 | 137.5 | 遇水剧烈水解,易与O2反应 |
POCl3 | 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于PCl3 |
SOCl2 | -105 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |
(1)若选用Na2SO3固体与70%浓H2SO4制取SO2,反应的离子方程式是:______________。
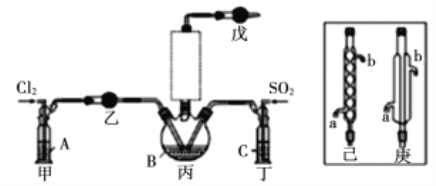
(2)溶液A为饱和食盐水,乙装置中应该盛装的试剂为__________(填“P2O5”或“碱石灰”或“浓H2SO4”或“无水硫酸铜”);反应装置图的虚框中未画出的仪器最好选择______(填“己”或“庚”)。
(3)甲、丁装置的作用除了用于气体的净化除杂外,还有_____________________________。
(4)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是_________________________。
(5)产品经提纯后仍含少量PCl3杂质,通过佛尔哈德法可测定产品中POCl3的含量:准确称取1.500g样品在碘量瓶中摇动至完全水解,将水解液配成100 mL溶液,取10.00 mL于锥形瓶中,加入0.2000 mol·L-1的AgNO3溶液20.00mL(Ag++C1-=AgC1↓),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖。加入NH4Fe(SO4)2作指示剂,用0.1000mol·L-1KSCN标准溶液滴定过量的AgNO3至终点(Ag++SCN-=AgSCN↓),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是_____________________________________________________。
②POCl3的质量分数为________________________。
③已知:KSP(AgC1)=3.2×10-10 mol2·L-2,KSP(AgSCN)=2×10-12 mol2·L-2,若无硝基苯覆盖沉淀表面,测定POCl3的质量分数将___________(填“偏大”、“偏小”、“无影响”)。