题目内容
9.已知铷(Rb)位于元素周期表中第五周期第ⅠA族,根据铷在元素周期表中的位置,推断下列内容:(1)铷的原子核外共有5层电子,最外层电子数为1,铷的原子序数为37.
(2)铷单质能与水剧烈反应,写出反应的化学方程式2Rb+2H2O=2RbOH+H2↑,.
(3)预测铷单质的还原性比钠单质的还原性强(填“弱”或“强”,下同),氢氧化铷的碱性比氢氧化钠的碱性强.
分析 (1)周期数等于电子层数,主族序数等于最外层电子数;
(2)同主族元素性质相似,与钠与水反应相似;
(3)同主族从上往下金属性增强,还原性增强,金属性越强最高价氧化物对应水化物的碱性越强;
解答 解:(1)周期数等于电子层数,主族序数等于最外层电子数,铷(Rb)位于元素周期表中第五周期第ⅠA族,所以铷的原子核外共有5个电子层,最外层电子数为1,铷的原子序数为36+1=37,故答案为:5;1;37;
(2)同主族元素性质相似,与钠与水反应相似,所以反应方程式为:2Rb+2H2O=2RbOH+H2↑,故答案为:2Rb+2H2O=2RbOH+H2↑;
(3)同主族从上往下金属性增强,还原性增强,金属性越强最高价氧化物对应水化物的碱性越强,所以铷单质的还原性比钠单质的还原性强,氢氧化铷的碱性比氢氧化钠的碱性强,故答案为:强;强.
点评 本题考查元素周期律的相关知识,学生要清楚同主族元素性质的变化规律这是解题的关键,比较容易.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
17.下列说法中,正确的是( )
| A. | 在光照条件下,体积比为1:1的CH4和Cl2充分反应可以制取CH3Cl | |
| B. | 乙烯和苯都可与溴水发生加成反应 | |
| C. | 用新制氢氧化铜可以检验淀粉是否完全水解 | |
| D. | 分子式同为C3H7Cl,但沸点不同的分子共有两种 |
4.中和滴定时,用于量取待测液体积的仪器是( )
| A. | 胶头滴管 | B. | 量筒 | C. | 滴定管 | D. | 移液管 |
14.在短周期元素中,甲元素与乙、丙、丁三种元素紧密相邻(上下左右均可能),四种元素的最外层电子数之和为24,甲、乙两元素的原子序数之和比丙元素的原子序数多1.下列说法中正确的是( )
| A. | 四种元素中,丁元素的原子半径最小 | |
| B. | 气态氢化物的稳定性:乙>丙 | |
| C. | 同浓度的最高价含氧酸溶液的H+浓度丁>丙 | |
| D. | 元素甲和丙形成的两种常见化合物均为强还原剂 |
1.下列仪器名称书写规范的是( )
| A. | 研钵 | B. | 溶量瓶 | C. | 三角架 | D. | 瓷坩锅 |
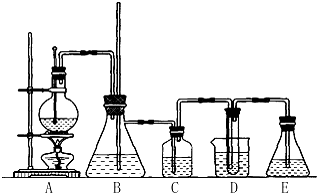
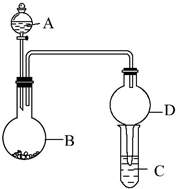 用如图所示装置进行实验(夹持装置已略去).请回答下列问题:
用如图所示装置进行实验(夹持装置已略去).请回答下列问题: