题目内容
11.下列实验装置能达到实验目的是(夹持仪器未画出)( )| A. | 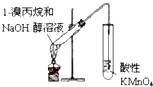 用于检验溴丙烷消去产物 | B. | 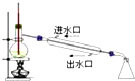 用于石油的分馏 | ||
| C. | 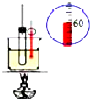 用于实验室制硝基苯 | D. | 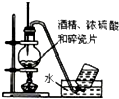 用于实验室制备乙烯 |
分析 A.乙醇和丙烯都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色;
B.石油分馏时,温度计测量馏分温度,且冷凝管中水采用逆流方法;
C.实验室用浓硝酸和苯制取硝基苯时,需要50-60℃;
D.实验室用浓硫酸和乙醇混合加热170℃制取乙烯.
解答 解:A.乙醇和丙烯都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,为防止乙醇干扰丙烯检验,应该先用水除去乙醇,然后用溴水或酸性高锰酸钾溶液检验丙烯,故A错误;
B.石油分馏时,温度计测量馏分温度,则温度计水银球应该位于蒸馏烧瓶支管口处,且冷凝管中水采用逆流方法,故B错误;
C.实验室用浓硝酸和苯制取硝基苯时,需要50-60℃,则要水浴加热,且温度计测量水浴温度,故C正确;
D.实验室用浓硫酸和乙醇混合加热170℃制取乙烯,温度计应该测量混合溶液温度,则水银球应该位于混合溶液中,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及实验操作、物质制备、物质检验等知识点,侧重考查实验操作及评价,明确实验原理、物质性质及操作规范性是解本题关键,注意温度计位置,为易错题.

练习册系列答案
相关题目
8.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,16g O2和32g O3的混合物中,含有O原子数月为3NA | |
| B. | 标准状况下,1mol Na2O和1mol Na2O2的混合物中,含有离子总数为7NA | |
| C. | 1 mol NaBH4中离子键的数目为2NA | |
| D. | 在K35ClO3+6H37Cl═KCl+3Cl2↑+3H2O中,若生成71 g Cl2,转移的电子数目为NA |
9.“凯氏定氮法”是测定化合物或混合物中总氮量的一种方法.近来,尿素化肥“金坷垃”在互联网上爆红.红星中学的化学实验小组成员想通过“凯氏定氮法”实验测定化肥“金坷垃”中的实际尿素含量,已检验它是否确实有网上所说的神奇功效.
实验流程如下:
金坷垃$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g“金坷垃”尿素[CO(NH2)2]化肥溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的金坷垃水溶液和辅助试剂,加热充分反应;
③将反应液转移到大试管中;
④按如图2装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);
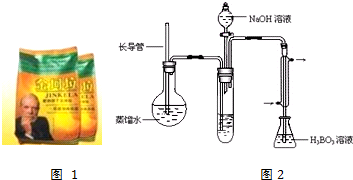
⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如表1:
表1
回答下列问题:
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得“金坷垃”化肥中的氮含量为117.67-3.5x克/每千克化肥(用含x的代数式表示,要求化简).我国农业用尿素的标准为:
表2
总尿素含量低于46.0%的为不合格品.若x=2.77,则根据上述测定,可以确定“金坷垃”尿素化肥属于不合格品级别.
实验流程如下:
金坷垃$→_{加热}^{辅助试剂}$(NH4)2SO4溶液$→_{吹出}^{NaOH}$NH3$→_{吸收}^{H_{3}BO_{3}}$(NH4)2B4O7溶液→用标准盐酸滴定
步骤:①取10.00g“金坷垃”尿素[CO(NH2)2]化肥溶于水,定容至100mL;
②在烧杯中加入10.00mL步骤①中得到的金坷垃水溶液和辅助试剂,加热充分反应;
③将反应液转移到大试管中;
④按如图2装置用水蒸气将NH3吹出,并用H3BO3溶液吸收(加热装置未画出);

⑤取下锥形瓶,滴加指示剂,用0.2500mol•L-1盐酸标准液滴定;
⑥重复实验操作.
数据记录如表1:
表1
| 实验编号 | 样品和辅助试剂 | 消耗盐酸体积(mL) |
| 1 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.45 |
| 2 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.90 |
| 3 | 10.00mL溶液、0.2g催化剂、20mL浓硫酸 | 33.50 |
| 4 | x |
(1)滴定时(NH4)2B4O7重新转化为H3BO3,反应的化学方程式为(NH4)2B4O7+2HCl+5H2O=4H3BO3+2NH4Cl.
(2)步骤③的实验装置中需要加热的仪器是圆底烧瓶(填仪器名称),长导管的作用是作为安全管,防止装置中压力过大而发生危险;防止冷却时发生倒吸.
(3)编号为4的实验应加入的样品和辅助试剂为10.00mL蒸馏水、0.2g催化剂、20mL浓硫酸,理由是空白、等量对照以消除其他试剂、实验操作等因素引起的误差.
(4)通过计算可得“金坷垃”化肥中的氮含量为117.67-3.5x克/每千克化肥(用含x的代数式表示,要求化简).我国农业用尿素的标准为:
表2
| 级别 | 优等品 | 一等品 | 合格品 |
| 总尿素含量%≥ | 46.4 | 46.2 | 46.0 |
6.已知等浓度溶液酸性:Al3+>H2CO3>HSO3->NH4+>HCO3-,下列有关反应正确的是( )
| A. | 向FeI2溶液中通入少量氯气:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 将少量CO2通入NH3•H2O中:CO2+2NH3•H2O═(NH4)2CO3+H2O | |
| C. | 将少量SO2通入NH3•H2O中:SO2+2NH3•H2O═(NH4)2SO3+H2O | |
| D. | 将AlCl3与等量Na2CO3溶液混合:3H2O+Al3++CO32-═HCO3-+Al(OH)3+2H+ |
3.下列关于σ键和π键的理解不正确的是( )
| A. | σ键能单独形成,而π键一定不能单独形成 | |
| B. | σ键可以绕键轴旋转,π键一定不能绕键轴旋转 | |
| C. | σ键比π键的重叠程度大,形成的共价键强 | |
| D. | CH3-CH3、CH2=CH2、CH≡CH中σ键都是C-C键,所以键能都相同 |
20.在m g 浓度为c mol•L-1,密度为ρ g/cm3的浓硫酸中加入一定量的水,稀释成浓度为c/2mol•L-1的硫酸,则加入水的体积为( )
| A. | 小于m mL | B. | 等于m mL | C. | 大于m mL | D. | 无法确定 |
1.用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 常温常压下,17g NH3所含有的原子的数目为4NA | |
| B. | 标准状况下,22.4LCCl4所含分子数为NA | |
| C. | 铝与足量盐酸反应,生成2.24LH2时,转移的电子数为0.2 NA | |
| D. | 0.1 mol/L的Na2CO3溶液中含有Na+的数目是0.2 NA |

 (1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.
(1)等质量的O2、CH4、H2的物质的量的比值为1:2+16.