题目内容
4.一定条件下,在一密闭容器中通人一定量SO2和O2的混合气,发生如下反应:2SO2(g)+O2(g)?2SO3(g)(正反应为放热反应).反应达平衡后SO2、O2和SO3的物质的量之比为3:4:6,若保持其他条件不变,降低温度后达到新的平衡时,O2和SO3的物质的量分别为1.1mol和2.0mol,则此时容器内SO2的物质的量应是( )| A. | 0.7 mol | B. | 0.9 mol | C. | 1.1 mol | D. | 1.3 mol |
分析 平衡体系中n(O)=2n(SO2)+3n(SO3)+2n(O2),n(S)=n(SO2)+n(SO3),原平衡时SO2、O2和SO3的物质的量之比为3:4:6,则平衡体系中n(S):n(O)=9:(6+8+18)=9:32.
解答 解:平衡体系中n(O)=2n(SO2)+3n(SO3)+2n(O2),n(S)=n(SO2)+n(SO3),原平衡时SO2、O2和SO3的物质的量之比为3:4:6,则平衡体系中n(S):n(O)=9:(6+8+18)=9:32,故[2mol+n(SO2)]:[2.2mol+6mol+2n(SO2)]=9:32,解得n(SO2)=0.7mol,
故选:A.
点评 本题考查化学平衡计算,侧重考查学生分析计算能力,注意利用原子守恒进行计算,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.2010年上海世博会的主题是“城市,让生活更美好”下列叙述不正确的是( )
| A. | 某些馆的外壳使用非晶硅薄膜,以充分利用太阳能 | |
| B. | 世博会期间,利用可降解的“主米塑料”替代一次性饭盒,可防止产生白色污染 | |
| C. | 世博会中国馆“东方之冠”使用的钢筋混凝土属于高分子化合物 | |
| D. | 世博停车场安装催化光解设施,可将汽车尾气中的CO和NO 转化为无毒气体CO2和N2 |
19.(1)将一定量的N2(g)和H2(g)放入2L的密闭容器中,在500℃、2×107Pa下发生如下反应:N2(g)+3H2(g)?2NH3(g)
①在反应体系中加入催化剂,反应速率增大,该反应的反应热不变(填“增大”、“减小”或“不变”).
②5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.氮气的平均反应速率v(N2)=0.01mol•L-1•min-1,H2的转化率为33.3%(保留小数点后一位).
③欲提高②容器中H2的转化率,下列措施可行的是AD.
A.把气体的体积压缩至1L B.向容器中再充入惰性气体
C.改变反应的催化剂 D.液化生成物分离出氨
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g)△H=a kJ/mol
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
此合成反应的a大于0.(填“大于”、“小于”或“等于”)
①在反应体系中加入催化剂,反应速率增大,该反应的反应热不变(填“增大”、“减小”或“不变”).
②5分钟后达到平衡,测得N2为0.2mol,H2为0.6mol,NH3为0.2mol.氮气的平均反应速率v(N2)=0.01mol•L-1•min-1,H2的转化率为33.3%(保留小数点后一位).
③欲提高②容器中H2的转化率,下列措施可行的是AD.
A.把气体的体积压缩至1L B.向容器中再充入惰性气体
C.改变反应的催化剂 D.液化生成物分离出氨
(2)根据最新“人工固氮”的研究报道,在常温、常压、光照条件下,N2在催化剂(掺有少量Fe2O3和TiO2)表面与水发生下列反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g)△H=a kJ/mol
进一步研究NH3生成量与温度关系,常压下达到平衡时测得部分实验数据如下:
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
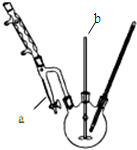 塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为:
塑化剂DBP(邻苯二甲酸二丁酯)主要应用于PVC等合成材料中作软化剂.反应原理为: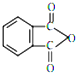 +2CH3CH2CH2CH2OH→
+2CH3CH2CH2CH2OH→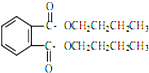 +H2O
+H2O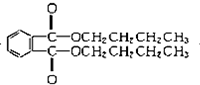 +2NaOH$\stackrel{△}{→}$
+2NaOH$\stackrel{△}{→}$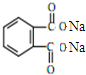 +2CH3CH2CH2CH2OH.
+2CH3CH2CH2CH2OH.