题目内容
下列各组混合气体中,含碳量比乙烯高的是( )
| A、甲烷和丙烯 |
| B、乙烷和乙烯 |
| C、乙烯和丙烯 |
| D、乙炔和丙烯 |
考点:元素质量分数的计算
专题:计算题,有机物分子组成通式的应用规律
分析:乙烯的最简式为CH2,把各物质的分子式转化成碳原子数为1的式子,H原子数目越大含碳量越低,再利用极限法来判断.
解答:
解:乙烯的最简式为CH2,
A、甲烷为CH4,含碳量比乙烯低,丙烯的最简式为CH2,含碳量与乙烯相等,所以甲烷和丙烯混合气体中含碳量比乙烯低,故A不符合;
B、乙烯的最简式都是CH2,乙烷的最简式为CH3,含碳量比乙烯低,二者混合含碳量比乙烯低,故B不符合;
C、乙烯、丙烯的最简式都是CH2,二者含碳量相等,二者混合含碳量不变,故C不符合;
D、乙炔最简式为CH,含碳量比乙烯高,丙烯的最简式为CH2,含碳量与乙烯相等,所以二者混合气体中含碳量比乙烯高,故D符合,
故选D.
A、甲烷为CH4,含碳量比乙烯低,丙烯的最简式为CH2,含碳量与乙烯相等,所以甲烷和丙烯混合气体中含碳量比乙烯低,故A不符合;
B、乙烯的最简式都是CH2,乙烷的最简式为CH3,含碳量比乙烯低,二者混合含碳量比乙烯低,故B不符合;
C、乙烯、丙烯的最简式都是CH2,二者含碳量相等,二者混合含碳量不变,故C不符合;
D、乙炔最简式为CH,含碳量比乙烯高,丙烯的最简式为CH2,含碳量与乙烯相等,所以二者混合气体中含碳量比乙烯高,故D符合,
故选D.
点评:本题主要考查混合物质量分数的判断,难度不大,注意利用分子式转化法及极限法进行解答.

练习册系列答案
相关题目
能正确表示下列反应的离子方程式的是( )
| A、氢氧化钡溶液与硫酸反应:H++OH-=H2O |
| B、铁溶于氯化铁溶液:Fe3++Fe=2Fe2+ |
| C、氢氧化钠溶液与硫酸铜溶液反应:2OH-+Cu2+=Cu(OH)2↓ |
| D、碳酸钙与盐酸反应:CO32-+2H+=CO2↑+H2O |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,48gO3和48gO2含有的氧原子数均为3NA |
| B、1.8g的NH4+离子中含有的电子数为0.1NA |
| C、11.2L氧气中所含有的原子数为NA |
| D、标准状况下,22.4 L水所含分子数为NA |
根据下列变化,判断属于还原反应的是( )
| A、HCl→Cl2 |
| B、S→SO2 |
| C、Fe(OH)3→Fe2O3 |
| D、CuO→Cu |
Se是人体必需的微量元素,其中
Se的原子棱内中子数是( )
80 34 |
| A、80 | B、46 | C、34 | D、12 |
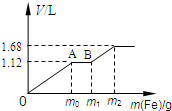 向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )
向50mL 稀H2SO4与稀HNO3的混合溶液中逐渐加入铁粉,假设加入铁粉的质量与产生气体的体积(标准状况)之间的关系如右图所示,且每一段只对应一个反应.下列说法正确的是( )| A、产生氢气的体积为1.68L |
| B、产生二氧化氮的体积为1.12L |
| C、参加反应铁粉的总质量m2=5.6g |
| D、原混合溶液中c(HNO3)=0.5 mol?L-1 |
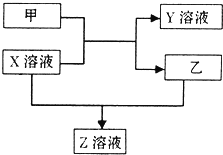 甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体.X、Y、Z是化合物.X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红.它们之间有如图所示转化关系.请回答:
甲、乙是同主族非金属元素组成的单质,乙通常状况下是深红棕色液体.X、Y、Z是化合物.X溶液呈淡绿色,Y、Z的溶液都能使KSCN溶液变红.它们之间有如图所示转化关系.请回答: