题目内容
11.以环戊烷为原料制备环戊二烯的合成路线如图,则( )
| A. | A的结构简式是 | |
| B. | ①②的反应类型分别是取代、消去 | |
| C. | 反应②③的条件分别是浓硫酸加热、光照 | |
| D. | 酸性KMnO4溶液褪色可证明  已完全转化成 已完全转化成  |
分析 以环戊烷为原料制备环戊二烯的合成路线为 ,反应①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生消去反应,反应③为加成反应,反应④为在氢氧化钠醇溶液中加热发生消去反应,以此来解答.
,反应①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生消去反应,反应③为加成反应,反应④为在氢氧化钠醇溶液中加热发生消去反应,以此来解答.
解答 解:以环戊烷为原料制备环戊二烯的合成路线为 ,
,
A.由上述分析可知,A为氯代环戊烷,故A错误;
B.反应①为光照条件下的取代反应,反应②为在氢氧化钠醇溶液中加热发生消去反应,故B正确;
C.反应②的反应试剂和反应条件为氢氧化钠醇溶液、加热,反应③的条件为常温,故C错误;
D.B为环戊烯,含碳碳双键,环戊二烯含碳碳双键,均能使高锰酸钾褪色,则酸性KMnO4溶液褪色不能证明环戊烷已完全转化成环戊二烯,故D错误;
故选B.
点评 本题考查有机物的合成及有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质分析,题目难度不大.

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
2.已知: ,
, 叫狄尔斯阿德而反应,用于构建六元环状烃,则下列说法不正确的是( )
叫狄尔斯阿德而反应,用于构建六元环状烃,则下列说法不正确的是( )
 ,
, 叫狄尔斯阿德而反应,用于构建六元环状烃,则下列说法不正确的是( )
叫狄尔斯阿德而反应,用于构建六元环状烃,则下列说法不正确的是( )| A. | 上述信息中反应的产物都可以使酸性高锰酸钾溶液褪色 | |
| B. | 通过上述反应合成 ,所需反应物为 2-甲基-1,3-丁二烯和乙烯 ,所需反应物为 2-甲基-1,3-丁二烯和乙烯 | |
| C. | 2-甲基-1,3-丁二烯和丙烯发生上述反应产物只有一种 | |
| D. | 2mol 环戊二烯发生上述反应的方程式为: |
19.下列叙述正确的是( )
| A. | 氯化钠溶液在电流作用下电离成钠离子和氯离子 | |
| B. | 溶于水后能电离出氢离子的化合物一定是酸 | |
| C. | 硫酸钡难溶于水,但硫酸钡属于电解质 | |
| D. | 氯气溶于水后的溶液能导电,故氯气属于电解质 |
6.在NO2被水吸收的反应中,发生还原反应和发生氧化反应的物质,其质量比为( )
| A. | 1:1 | B. | 1:3 | C. | 1:2 | D. | 4:1 |
16.加热金属Cu与浓硫酸反应,得到SO2的体积为2.24L(标准状况).则( )
| A. | 被还原的H2SO4为0.2moL | |
| B. | 反应中共转移电子0.1moL | |
| C. | 反应消耗了金属Cu6.4g | |
| D. | 生成的CuSO4配成500mL溶液,浓度为1mol/L |
3.实验室常用氯化铵与氢氧化钙的固体混合物加热制取氨气,该反应的化学方程式为:2NH4Cl+Ca(OH)2$\stackrel{△}{→}$CaCl2+2NH3↑+2H2O.下列是实验室提供的有关装置:
(1)请从图中选择实验室制取氨气的气体发生装置b(填序号)、气体收集装置①(填序号).
(2)某学生用100mL注射器收集了50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后,注射器内无(填“有”或“无”)气体剩余,其中的液体呈红色,请用方程式解释液体颜色变化的原因:NH3+H2O?NH3•H2O?NH4++OH-.
(3)氨具有广泛的用途,它可用于制造化肥/制造硝酸/作冷却剂(举出一种即可).工业上合成氨常常要用铁触媒作催化剂,所加催化剂能否提高N2的转化率不能.理由是催化剂只改变化学反应速率,不影响平衡移动.
(4)工业合成氨的简易流程如下:

通过循环Ⅰ可利用的气态物质是D
A.催化剂 B.只有N2C.只有H2 D.N2和H2.
| 气体发生装置 | 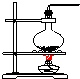 a |  b | 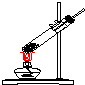 c |
| 气体收集装置 | 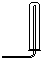 ① |  ② | 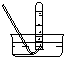 ③ |
(2)某学生用100mL注射器收集了50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后,注射器内无(填“有”或“无”)气体剩余,其中的液体呈红色,请用方程式解释液体颜色变化的原因:NH3+H2O?NH3•H2O?NH4++OH-.
(3)氨具有广泛的用途,它可用于制造化肥/制造硝酸/作冷却剂(举出一种即可).工业上合成氨常常要用铁触媒作催化剂,所加催化剂能否提高N2的转化率不能.理由是催化剂只改变化学反应速率,不影响平衡移动.
(4)工业合成氨的简易流程如下:

通过循环Ⅰ可利用的气态物质是D
A.催化剂 B.只有N2C.只有H2 D.N2和H2.
 A、B、C、D均为含苯环的有机物,且式量B>A>C.
A、B、C、D均为含苯环的有机物,且式量B>A>C. .
. .
. 、
、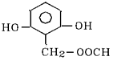 、
、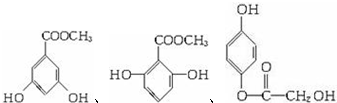 (其中的任意2种).
(其中的任意2种).