题目内容
12.氧化铁俗称铁红,可用于水泥制件、橡胶制品、塑料制品的着色,在工业上有广泛的用途,某工厂采用生产钦白粉的下脚料(含大量FeSO4的废液)为原料来制备氧化铁.
已知煅烧过程中的化学反应方程式为:FeCO3→FeO+CO2↑,4FeO+O2→2Fe2O3
(1)用98%的H2SO4配制20%的H2SO4,所需玻璃仪器除量筒外还有BD
A.容量瓶 B.烧杯 C.烧瓶 D.玻璃棒
(2)向下脚料废液中加入铁皮的作用是(用有关的离子方程式表示)2Fe3++Fe=3Fe2+
(3)加入20%H2SO4的作用是抑制Fe2+的水解
(4)浓缩结晶后得到的晶体是FeSO4•7H2O (填化学式),A中所含的离子除H+、OH-、NH4+外,还含有大量的SO42-,检验该离子的方法是加盐酸酸化的氯化钡溶液,如果有白色沉淀生成,表示溶液中含有硫酸根.
(5)写出步骤“合成”中发生的化学变化(用化学方程式表示)FeSO4+2NH4HCO3=FeCO3↓+( NH4)2SO4+CO2↑+H2O.
分析 (1)依据配制一定溶质质量分数的方法解答;
(2)下脚料中含有硫酸亚铁,向稀硫酸、铁片发生反应生成硫酸亚铁;
(3)硫酸亚铁为强酸弱碱盐,水解显酸性;
(4)下脚料中含有硫酸亚铁,向稀硫酸、铁片发生反应生成硫酸亚铁,且稀硫酸能抑制硫酸亚铁水解,然后向溶液中加入絮凝剂和水,得到吸附杂质的絮凝剂,然后过滤得到滤液,浓缩结晶滤液,得到FeSO4•7H2O,然后向溶液中加入碳酸氢铵,发生的反应为FeSO4+2NH4HCO3=FeCO3↓+( NH4)2 SO4+CO2↑+H2O,然后洗涤过滤得到A,滤液A为(NH4)2 SO4,根据硫酸根离子的检验方法检验;
(5)硫酸亚铁与 碳酸氢铵反应生成碳酸铁、硫酸铵和二氧化碳、水.
解答 解:(1)配制一定溶质质量分数溶液的方法是:计算、称量、溶解,用到的仪器有:烧杯、玻璃棒,故选:BD;
(2)下脚料中含有硫酸亚铁,向稀硫酸、铁片发生反应生成硫酸亚铁,离子方程式为:2Fe3++Fe=3Fe2+,故答案为:2Fe3++Fe=3Fe2+;
(3)硫酸亚铁为强酸弱碱盐,水解显酸性,所以要保存硫酸亚铁不变质,应加入硫酸,硫酸作用是抑制Fe2+的水解,故答案为:抑制Fe2+的水解;
(4)下脚料中含有硫酸亚铁,向稀硫酸、铁片发生反应生成硫酸亚铁,且稀硫酸能抑制硫酸亚铁水解,然后向溶液中加入絮凝剂和水,得到吸附杂质的絮凝剂,然后过滤得到滤液,浓缩结晶滤液,得到FeSO4•7H2O,然后向溶液中加入碳酸氢铵,发生的反应为FeSO4+2NH4HCO3=FeCO3↓+( NH4)2 SO4+CO2↑+H2O,然后洗涤过滤得到A,滤液A为(NH4)2 SO4,硫酸根离子的检验方法是:加盐酸酸化的氯化钡溶液,如果有白色沉淀生成,表示溶液中含有硫酸根,故答案为:FeSO4•7H2O;SO42-;加盐酸酸化的氯化钡溶液,如果有白色沉淀生成,表示溶液中含有硫酸根;
(5)硫酸亚铁与 碳酸氢铵反应生成碳酸铁、硫酸铵和二氧化碳、水,化学方程式:FeSO4+2NH4HCO3→FeCO3↓+( NH4)2 SO4+CO2↑+H2O;
故答案为:FeSO4+2NH4HCO3→FeCO3↓+( NH4)2 SO4+CO2↑+H2O.
点评 本题通过氧化铁的制备为载体考查了化学方程式的书写、离子浓度大小比较、盐类水解的应用,题目难度中等.

| A. | 元素X与Z、Y 与W形成的化合物都为离子化合物 | |
| B. | 元素X与Y,Z与Y形成的二元化合物都只有一种 | |
| C. | Y、Z、W三种元素形成的离子半径随原子序数的增加而增大 | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
| A. | ν(H2)=0.03 mol•L-1•min-1 | B. | ν(NH3)=1.7 g•L-1•min-1 | ||
| C. | ν(N2)=0.02 mol•L-1•min-1 | D. | ν(NH3)=0.01 mol•L-1•min-1 |
| A. | FeO、Fe2O3 | B. | FeO、Fe3O4 | C. | Fe2O3、Fe3O4 | D. | FeO、Fe2O3、Fe3O4 |

有关物质沸点数据
| 物质 | 沸点 |
| 乙醚 | 34.6℃ |
| 乙醇 | 78.2℃ |
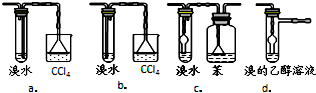
①Ⅰ和Ⅱ是反应发生装置,应该选择Ⅰ(选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连.
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是防止乙醇挥发.
③Ⅲ中水冷凝管的进水口是b(选答“a”或“b”).冰盐水的作用是凝液化乙醚.
④有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险.该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号)c、d.
⑤反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色.写出实验过程中有气体生成的化学方程式(写两个方程式)CH3CH2OH+6H2SO4$\stackrel{△}{→}$2CO2↑+6SO2↑+↑+2H2O;C+2H2SO4$\stackrel{△}{→}$CO2↑+2SO2↑+2H2O、CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O、CH3CH2OH+2H2SO4$\stackrel{△}{→}$2C+2SO2↑+5H2O(其中两个).
⑥实验中收集到的乙醚产品中可能含有多种杂质.某同学设计了以下提纯方案:

(2)分液步骤除去产品中的酸性杂质,则X可以是NaOH.
(3)蒸馏操作可除去的杂质是乙醇(CH3CH2OH).
| A. | 有机化合物主要来自自然界众多的有机体 | |
| B. | 有机物分子中的碳原子成键方式具有多样性 | |
| C. | 可以人工合成 | |
| D. | 可以由无机物进行转化 |
| A. | 通过溴水 | B. | 通过溴的四氯化碳溶液 | ||
| C. | 通过酸性KMnO4溶液 | D. | 在催化剂加热时通入氢气 |
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 氮氧化物 | D. | 可吸入颗粒物 |
 ,
,
 的同分异构体:
的同分异构体: 、
、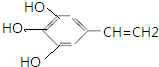 .
.