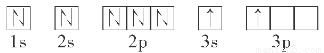题目内容
我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应如下:HCHO+O2 CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.该反应为吸热反应
B.CO2分子中的化学键为非极性键
C.HCHO分子中既含σ键又含π键
D.每生成1.8 g H2O消耗2.24 L O2
C
【解析】从题给信息入手分析,结合原子成键特点,在准确理解相关概念的前提下进行判断。
A.通过分析化学方程式可知,该反应等同于甲醛的燃烧,属于放热反应。B.CO2的结构式为O=C=O,可见CO2中的共价键是由不同元素的原子形成的,属于极性键。C.甲醛中碳原子采取sp2杂化,有三个等同的sp2杂化轨道伸向平面三角形的三个顶点,分别形成3个σ键,一个未参加杂化的p轨道与O原子的2p轨道形成π键。D.根据题给化学方程式可知,每生成1.8 g水消耗0.1 mol氧气,但由于题中并没有给出温度和压强,所以不能确定氧气的体积一定为2.24 L。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
实验编号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
下列判断不正确的是( )
A.实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+)
B.实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)= mol/L
mol/L
C.实验②反应后的溶液中:c(A-)+c(HA)>0.1 mol/L
D.实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+)