题目内容
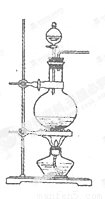
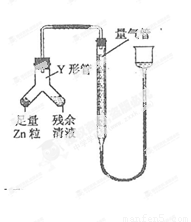
①用过量的锌与浓H2SO4反应某同学认为除了生成二氧化硫外.还有氢气产生,理由________。②用过量铜片0.2 mol与浓H2SO4共热足够长时间(只考虑铜与浓H2SO4反应,忽略其他副反应),甲认为产生的SO2少于0.1 mol,理由是________,而乙同学认为产生的SO2恰为0.1mol,理由是________。
答案:
解析:
解析:
| ①由于Zn过量,随着反应的进行,浓H2SO4变稀,稀H2SO4可与Zn反应产生H2。②(甲)由于反应Cu+2H2SO4======CuSO4+SO2↑十2H2O,知0.2 mol H2SO4全部反应时,才生成0.1 mol SO2,随反应进行,浓H2SO4变稀,而稀H2SO4与铜不反应。(乙)由于加热时间足够长,水比硫酸易挥发,因此硫酸始终保持较高浓度,直至与铜反应完为止。
|

练习册系列答案
相关题目
 (2012?福建)实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图1所示).
(2012?福建)实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图1所示).