题目内容
按要求写出化学方程式:
(1)对二甲苯与足量H2在Ni作催化剂,加热、加压时发生反应:
(2)甲苯与浓硝酸、浓硫酸混合后在100℃时发生反应:
(3)腈纶(人造羊毛)的主要成分是聚丙烯腈(丙烯腈CH2=CH-CN),试写出合成它的化学方程式: .
(1)对二甲苯与足量H2在Ni作催化剂,加热、加压时发生反应:
(2)甲苯与浓硝酸、浓硫酸混合后在100℃时发生反应:
(3)腈纶(人造羊毛)的主要成分是聚丙烯腈(丙烯腈CH2=CH-CN),试写出合成它的化学方程式:
考点:化学方程式的书写,苯的同系物
专题:有机物的化学性质及推断
分析:(1)苯环中的碳碳键位于单、双键之间,是一种独特的化学键,能发生加成反应;
(2)甲苯与浓硫酸和浓硝酸的混酸加热反应生成2,4,6-三硝基甲苯和水,发生的是取代反应;
(3)含有碳碳双键的物质能发生加聚反应,丙烯腈CH2=CH-CN发生加聚反应,生成聚丙烯腈.
(2)甲苯与浓硫酸和浓硝酸的混酸加热反应生成2,4,6-三硝基甲苯和水,发生的是取代反应;
(3)含有碳碳双键的物质能发生加聚反应,丙烯腈CH2=CH-CN发生加聚反应,生成聚丙烯腈.
解答:
解:(1)对二甲苯与足量H2在Ni作催化剂,加热、加压时发生加成反应,反应为: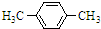 +3H2
+3H2
 ,
,
故答案为: +3H2
+3H2
 ;
;
(2)甲苯与浓硫酸和浓硝酸的混酸加热发生取代反应,生成2,4,6-三硝基甲苯和水,反应的化学方程式为: ,
,
故答案为: ;
;
(3)含有碳碳双键的有机物能发生加聚反应,丙烯腈含有碳碳双键能发生加聚反应,nCH2=CH-CN
 ,
,
故答案为:nCH2=CH-CN
 .
.
 +3H2
+3H2| Ni |
| 加热、加压 |
 ,
,故答案为:
 +3H2
+3H2| Ni |
| 加热、加压 |
 ;
;(2)甲苯与浓硫酸和浓硝酸的混酸加热发生取代反应,生成2,4,6-三硝基甲苯和水,反应的化学方程式为:
 ,
,故答案为:
 ;
;(3)含有碳碳双键的有机物能发生加聚反应,丙烯腈含有碳碳双键能发生加聚反应,nCH2=CH-CN
| 引发剂 |
 ,
,故答案为:nCH2=CH-CN
| 引发剂 |
 .
.
点评:本题考查化学反应方程式的书写,明确物质含有的官能团是解本题的关键,题目难度不大.

练习册系列答案
相关题目
下列化学用语对应正确的是( )
A、CH4分子的比例模型: |
B、CCl4的电子式: |
| C、H2O2的结构式:H-O-O-H |
| D、乙酸的最简式:C2H4O2 |
化学与科学、技术、社会、环境、生活等密切相关.下列有关说法中错误的是( )
| A、液氨可用作制冷剂 |
| B、小苏打用于治疗胃酸过多 |
| C、明矾可用于自来水的杀菌消毒 |
| D、硅酸钠用于制备硅胶和木材防火剂的原料 |
 中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:
中国环境监测总站数据显示,颗粒物(PM2.5等)为连续雾霾过程影响空气质量最显著的污染物,其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义.请回答下列问题:

