题目内容
下列化学用语对应正确的是( )
A、CH4分子的比例模型: |
B、CCl4的电子式: |
| C、H2O2的结构式:H-O-O-H |
| D、乙酸的最简式:C2H4O2 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.甲烷为正四面体结构,比例模型能够体现出甲烷中各原子的相对体积大小,题中为甲烷的球棍模型;
B.四氯化碳的电子式中,氯原子最外层为8个电子;
C.双氧水中存在2个氧氢键和应该氧氧键,据此写出其结构式;
D.乙酸分子中含有官能团羧基,其结构简式中没有标出官能团羧基.
B.四氯化碳的电子式中,氯原子最外层为8个电子;
C.双氧水中存在2个氧氢键和应该氧氧键,据此写出其结构式;
D.乙酸分子中含有官能团羧基,其结构简式中没有标出官能团羧基.
解答:
解:A. 为甲烷的球棍模型,甲烷的比例模型能够表示出碳原子与氢原子体积的相对大小,甲烷正确的比例模型为:
为甲烷的球棍模型,甲烷的比例模型能够表示出碳原子与氢原子体积的相对大小,甲烷正确的比例模型为: ,故A错误;
,故A错误;
B.四氯化碳为共价化合物,分子中碳原子和氯原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为: ,故B错误;
,故B错误;
C.双氧水的电子式为: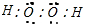 ,将所有共用电子对用短线表示即为双氧水的结构式,双氧水的结构式为:H-O-O-H,故C正确;
,将所有共用电子对用短线表示即为双氧水的结构式,双氧水的结构式为:H-O-O-H,故C正确;
D.乙酸分子的官能团为羧基,乙酸的结构简式必须标出其官能团,乙酸正确的结构简式为:CH3COOH,故D错误;
故选C.
 为甲烷的球棍模型,甲烷的比例模型能够表示出碳原子与氢原子体积的相对大小,甲烷正确的比例模型为:
为甲烷的球棍模型,甲烷的比例模型能够表示出碳原子与氢原子体积的相对大小,甲烷正确的比例模型为: ,故A错误;
,故A错误;B.四氯化碳为共价化合物,分子中碳原子和氯原子最外层都达到8电子稳定结构,四氯化碳正确的电子式为:
 ,故B错误;
,故B错误;C.双氧水的电子式为:
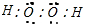 ,将所有共用电子对用短线表示即为双氧水的结构式,双氧水的结构式为:H-O-O-H,故C正确;
,将所有共用电子对用短线表示即为双氧水的结构式,双氧水的结构式为:H-O-O-H,故C正确;D.乙酸分子的官能团为羧基,乙酸的结构简式必须标出其官能团,乙酸正确的结构简式为:CH3COOH,故D错误;
故选C.
点评:本题考查了常见化学用语的判断,题目难度中等,注意掌握比例模型与球棍模型、电子式、结构简式、结构式等化学用语的概念及判断方法,明确球棍模型与比例模型的区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法或做法错误的是( )
| A、充满NH3的烧瓶倒置于水中后液面迅速上升,说明NH3易溶于水 |
| B、在胆矾中滴加浓H2SO4,固体变白,说明浓H2SO4具有吸水性 |
| C、将二氧化硫通入品红溶液,溶液褪色,加热后能恢复原色 |
| D、向铜粉中加入浓硫酸,加热,铜粉溶解,同时产生H2 |
下列关于有机物存在的叙述,错误的是( )
| A、工业酒精中含有乙醇和甲醇 |
| B、煤中含有苯和甲苯 |
| C、天然油脂中含有高级脂肪酸甘油酯 |
| D、许多水果中含有酯类化合物 |
下列说法正确的是( )
| A、在纯水中加入醋酸会促进水的电离 |
| B、1mL pH=2的醋酸稀释至10mL,pH=3 |
| C、常温下,0.1mol?L-1氯化铵溶液加水稀释,溶液中所有离子浓度均减小 |
| D、加热Na2CO3溶液能提高其除油污的能力 |
下列说法正确的是( )
| A、冰熔化时,分子中H-O键发生断裂 |
| B、NaOH中只含有离子键 |
| C、CO2与SiO2都属于分子晶体 |
| D、熔沸点由高到低的顺序是金刚石>NaCl>I2 |
在0.1mol/L的氨水中存在如下电离平衡:NH3?H2O?NH4++OH-,对于该平衡,下列叙述正确的是( )
| A、通入少量HCl气体,平衡向逆反应方向移动 |
| B、加水,反应速率加快,平衡向逆反应方向移动 |
| C、滴加少量0.1mol/L NaOH溶液,溶液中c(OH-)减少 |
| D、加入少量NH4Cl固体,平衡向逆反应方向移动 |
如图图所示的装置中,有关说法不正确的是( )


| A、该装置实现化学能转变为电能 |
| B、该装置中Cu2+向Zn电极移动 |
| C、该装置外电路中电子由Zn棒转移到Cu棒 |
| D、该装置中Zn棒上的电极反应为:Zn-2e-═Zn2+ |
