题目内容
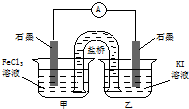 控制条件,能将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法正确的是( )
控制条件,能将反应2Fe3++2I-?2Fe2++I2设计成如图所示的原电池.下列说法正确的是( )分析:根据常温下能自动发生的氧化还原反应都可设计成原电池,再利用正反应2Fe3++2I-?2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极,利用负极发生氧化反应,正极发生还原反应,并利用平衡移动来分析解答.
解答:解:A.反应开始时,因乙中I-失去电子放电,元素的化合价升高,则发生氧化反应,故A错误;
B.氯化铁电极为正极,碘化钾电极为负极,盐桥中阳离子向正极移动,所以向氯化铁溶液中迁移,故B错误;
C.当电流计为零时,说明没有电子发生转移,则反应达到平衡,故C正确;
D.当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D错误,
故选C.
B.氯化铁电极为正极,碘化钾电极为负极,盐桥中阳离子向正极移动,所以向氯化铁溶液中迁移,故B错误;
C.当电流计为零时,说明没有电子发生转移,则反应达到平衡,故C正确;
D.当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,故D错误,
故选C.
点评:本题考查了原电池原理,根据电池反应式确定正负极,并注重与化学平衡移动原理联系起来分析解答,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 (1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
(1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=