题目内容
(1)已知:2SO2(g)+O2(g)?2SO3 (g)△H=-196.6kJ?mol-1;2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1 .则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
一定条件下,将NO2与SO2 按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
a.体系压强保持不
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
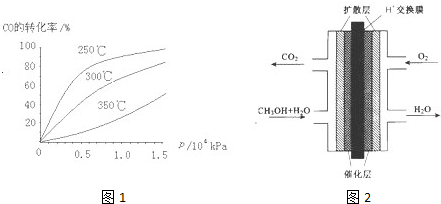
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H
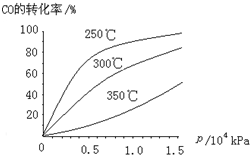
(3)甲醇(CH3OH)燃料电池的结构示意图如图2.甲醇进入
(4)101kPa时,若16gCH3OH完全燃烧生成液态水,放出热量为363.25kJ/mol,则甲醇燃烧的热化学方程式为
-41.8
-41.8
kJ?mol-1一定条件下,将NO2与SO2 按体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是
b
b
.a.体系压强保持不
b.混合气体颜色保持不变
c.SO3与NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
(2)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)?CH3OH(g).CO在不同温度下的平衡转化率与压强的关系如图1所示.该反应△H
<
<
0(填“>”或“<”).实际生产条件控制在250℃、1.3×104kPa左右,选择此压强的理由是在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失
在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失

(3)甲醇(CH3OH)燃料电池的结构示意图如图2.甲醇进入
负
负
极(填“正”或“负”),正极发生的电极反应为O2+4H++4e-═2H2O
O2+4H++4e-═2H2O
.(4)101kPa时,若16gCH3OH完全燃烧生成液态水,放出热量为363.25kJ/mol,则甲醇燃烧的热化学方程式为
CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol
CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol
.分析:(1)依据盖斯定律结合热化学方程式计算得到所求的热化学方程式;化学平衡状态的标志的本质是正逆反应速率相等,各组分浓度或含量不变;根据化学平衡状态的特征:逆、定、动、变、等来判断化学反应是否达到平衡;
(2)利用化学平衡的影响因素和工业生产的关系来分析;
(3)甲醇燃料电池中,甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳;正极是氧气得到电子生成水;
(4)依据化学方程式甲醇物质的量结合题干条件计算得到对应量下的焓变,标注物质聚集状态和对应焓变,写出热化学方程式.
(2)利用化学平衡的影响因素和工业生产的关系来分析;
(3)甲醇燃料电池中,甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳;正极是氧气得到电子生成水;
(4)依据化学方程式甲醇物质的量结合题干条件计算得到对应量下的焓变,标注物质聚集状态和对应焓变,写出热化学方程式.
解答:解:(1)根据盖斯定律,将第二个方程式颠倒过来,与第一个方程式相加得:2NO2+2SO2═2SO3+2NO,△H=-83.6 kJ?mol-1,则NO2+SO2?SO3+NO,△H=-41.8 kJ?mol-1;
a、本反应是反应前后气体分子数不变的反应,故体系的压强保持不变,故a不能说明反应已达到平衡状态;
b、随着反应的进行,NO2的浓度减小,颜色变浅,故b可以说明反应已达平衡;
c、SO3和NO都是生成物,比例保持1:1,故c不能作为平衡状态的判断依据;
d、d中所述的两个速率都是逆反应速率,不能作为平衡状态的判断依据;故选b;
故答案为:-41.8;b;
(2)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强,
故答案为:<;在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失;
(3)甲醇燃料电池中,甲醇中C元素的化合价升高,则甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳,电极反应为CH3OH+H2O-6e-=CO2+6H+,氧气再正极上得到电子发生还原反应在酸溶液中生成水,反应的电极反应为:O2+4H++4e-═2H2O,
故答案为:负; O2+4H++4e-═2H2O;
(4)101kPa时,若16gCH3OH物质的量为0.5mol,完全燃烧生成液态水,放出热量为363.25kJ/mol,则1mol甲醇燃烧放热726.5KJ;反应的热化学方程式为:CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol,
故答案为:CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol.
a、本反应是反应前后气体分子数不变的反应,故体系的压强保持不变,故a不能说明反应已达到平衡状态;
b、随着反应的进行,NO2的浓度减小,颜色变浅,故b可以说明反应已达平衡;
c、SO3和NO都是生成物,比例保持1:1,故c不能作为平衡状态的判断依据;
d、d中所述的两个速率都是逆反应速率,不能作为平衡状态的判断依据;故选b;
故答案为:-41.8;b;
(2)由图可知,温度升高,CO的转化率降低,平衡向逆反应方向移动,故逆反应是吸热反应,正反应是放热反应,△H<0;压强大,有利于加快反应速率,有利于使平衡正向移动,但压强过大,需要的动力大,对设备的要求也高,故选择250℃、1.3×104kPa左右的条件.因为在250℃、压强为1.3×104 kPa时,CO的转化率已较大,再增大压强,CO的转化率变化不大,没有必要再增大压强,
故答案为:<;在1.3×104kPa下,CO的转化率已较高,再增大压强CO的转化率提高不大,而生产成本增加得不偿失;
(3)甲醇燃料电池中,甲醇中C元素的化合价升高,则甲醇为负极,电解质为酸,甲醇失去电子生成二氧化碳,电极反应为CH3OH+H2O-6e-=CO2+6H+,氧气再正极上得到电子发生还原反应在酸溶液中生成水,反应的电极反应为:O2+4H++4e-═2H2O,
故答案为:负; O2+4H++4e-═2H2O;
(4)101kPa时,若16gCH3OH物质的量为0.5mol,完全燃烧生成液态水,放出热量为363.25kJ/mol,则1mol甲醇燃烧放热726.5KJ;反应的热化学方程式为:CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol,
故答案为:CH3OH(l)+3/2 O2(g)═CO2(g)+2H2O(l)△H=-726.5 kJ/mol.
点评:本题考查了盖斯定律计算应用,热化学方程式的书写,化学平衡标志判断,原电池原理的应用,该题将元素化合物与能量变化、化学平衡等知识柔和在一起进行考查,充分体现了高考的综合性,看似综合性较强的问题,只要细细分析,还是能各个突破的.第(2)容易出错,需认真分析图象,得出正确结论,题目难度中等.

练习册系列答案
相关题目
 (1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=
(1)已知:2SO2(g)+O2(g)?2SO3(g)△H=-196.6kJ?mol-1,2NO(g)+O2(g)?2NO2(g)△H=-113.0kJ?mol-1,则反应NO2(g)+SO2(g)?SO3(g)+NO(g)的△H=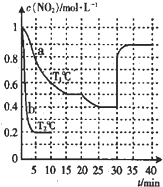 (2012?百色二模)在2L的密闭容器内投入一定量NO2,发生反应2NO2(g)?2NO(g)+O2(g).分别在a、b两种不同实验条件下反应,得出NO2的浓度随时间变化的曲线如图所示.
(2012?百色二模)在2L的密闭容器内投入一定量NO2,发生反应2NO2(g)?2NO(g)+O2(g).分别在a、b两种不同实验条件下反应,得出NO2的浓度随时间变化的曲线如图所示.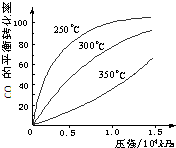 Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.
Ⅰ.研究NO2、SO2、CO等大气污染气体的处理具有重要意义.